
【题目】下列表格中各项分类都正确的一组是( )
纯净物 | 混合物 | 电解质 | 非电解质 | |
A | 冰水混合物 | CuSO45H2O | 液态KNO3 | 蔗糖 |
B | CaO | 海水 | 铜 | 酒精 |
C | 液氯 | 铝合金 | AgCl | CO2 |
D | 氢氧化钠 | 空气 | Na2SO4溶液 | 食醋 |
A.A
B.B
C.C
D.D
科目:高中化学 来源: 题型:
【题目】在任何条件下,纯水显中性,这是因为
A.pH=7 B.c(H +)=c(OH -)
C.c(H+)=c(OH-)=10-7mol·L-1 D.c(H +)×c(OH-)=10-14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室用浓盐酸和二氧化锰反应制取氯气时,反应为4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O收集到7.1g氯气,求:
MnCl2+Cl2↑+2H2O收集到7.1g氯气,求:
①发生反应的二氧化锰的物质的量是多少?
②被氧化的氯化氢的物质的量是多少?
(2)把5.1g镁铝合金粉末放入500mL 1mol/L盐酸中,恰好完全反应。试计算:
①该合金中镁和铝的物质的量各为多少mol。
②将等质量的该合金投入足量的氢氧化钠溶液中,求标况下放出气体的体积。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙为常见单质。A、B、C、D、E、F、G、H均为中学化学中常见的化合物,其中B、G的焰色反应均为黄色,C能使品红溶液褪色。在一定条件下,各物质相互转化关系如图所示。

请回答下列问题:
(1)用化学式表示:丙为 ,H为 。
(2)A的电子式为 。
(3)写出B+C→D的化学方程式 。
写出E+G→F的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mL某混合溶液中,c(HNO3)=0.4mol/L,c(H2SO4)=0.1mol/L,向其中加入 1.92g铜粉,微热,充分反应后溶液中c(Cu2+)为
A.0.15mol/L B.0.3mol/L C.0.225mol/L D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ΔH=-746.8 kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是
2CO2(g)+N2(g) ΔH=-746.8 kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是
A.降低温度 B.升高温度同时充入N2
C.增大压强同时加催化剂 D.及时将CO2和N2从反应体系中移走
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O
B.向Ca(HCO3)2溶液中加入足量的氢氧化钠溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O
C.向KHSO4溶液中滴入Ba(OH)2溶液恰好中性:SO42-+H++Ba2++OH-=BaSO4↓+H2O
D.向沸水中滴入饱和氯化铁溶液制取Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学―选修2:化学与技术】以硫铁矿(主要成分为FeS2)为原料制取硫酸,其矿渣可用来炼铁。生产工艺示意图如下:
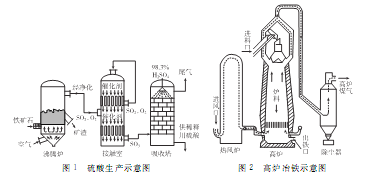
(1)配平煅烧硫铁矿的反应方程式:______FeS2+________O2→_____Fe2O3+______SO2。实际生产中向沸腾炉通入的空气量要大于锻烧硫铁矿所需空气量.其目的是____________________。接触室和热风炉中都装有热交换器,可用反应的余热将通入的气体加热,这样做的好处是_____________________。
(2)生产硫酸时,吸收塔中用98.3%的硫酸吸收而不用水吸收SO3的原因是______________。用含FeS280%的硫铁矿生产硫酸,如果煅烧时有5%的硫损失,SO2转变成SO3的转化率为80%,那么生产98%的浓硫酸3吨,则需要这种硫铁矿___________吨。
(3)CO还原Fe2O3的冶铁过程中,反应物、生成物和温度之间的关系如图所示.
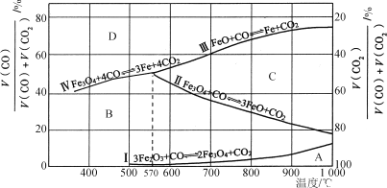
(图中Ⅰ、Ⅱ、Ⅲ、Ⅳ四条曲线是四个化学反应平衡时的气相组成对温度作图得到的;A、B、C、D四个区域分别是Fe2O3、Fe3O4、FeO、Fe稳定存在的区域)
①冶炼高炉产生的高炉煤气的主要成分有__________和剩余的CO。
②据图分析,下列说法正确的是________(填字母)。
a.温度低于570 ℃时,Fe2O3还原焙烧的产物中不含FeO
b.温度越高,Fe2O3还原焙烧得到的固体物质组成中Fe元素的质量分数越高
c.Fe2O3还原焙烧过程中及时除去CO2有利于提高Fe的产率
③800℃时,混合气体中CO2体积分数为40%时,Fe2O3用CO还原焙烧反应的化学方程式为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com