
| A. | 反应速率用于衡量化学反应进行的快慢 | |
| B. | 决定反应速率的主要因素是反应物的性质 | |
| C. | 增大反应物的浓度、提高反应温度都能增大反应速率 | |
| D. | 可逆反应达到化学平衡状态时,正、逆反应的速率都为0 |
分析 影响化学反应速率的因素有内因和外因,内因为主要因素,化学反应速率可衡量化学反应的快慢,而反应限度用于衡量反应的程度,达到反应限度时,正逆反应速率相等,外界条件发生改变,平衡发生移动,以此解答该题.
解答 解:A.化学反应速率为单位时间内浓度的变化,可衡量化学反应的快慢,故A正确;
B.影响化学反应速率的因素有内因和外因,内因为物质的性质,为影响反应速率的主要因素,故B正确;
C.增大反应物浓度,化学反应速率增大;升高温度,化学反应速率增大,故C正确;
D.可逆反应达到平衡时,正逆反应速率相等,且不等于0,故D错误.
故选D.
点评 本题考查化学反应速率的影响因素,为高频考点,侧重于学生的分析能力和基础知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大,注意把握影响化学反应速率的因素与影响原因的关系.


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-38 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 结晶牛胰岛素 | B. | 氰酸铵 | C. | 葡萄糖 | D. | 尿素 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
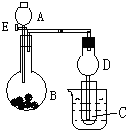 用如图所示装置进行实验,将A逐滴加入B中:
用如图所示装置进行实验,将A逐滴加入B中:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
类别 选项 | 纯净物 | 混合物 | 电解质 | 非电解质 |
| A | 生理盐水 | 明矾 | 液态KNO3 | 蔗糖 |
| B | CaO | 海 水 | 铜 | 乙醇 |
| C | 胆矾 | 铝合金 | AgCl | CO2 |
| D | 氢氧化钠 | 空气 | Na2SO4溶液 | 食醋 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:10:104:109 | B. | 1:5:5×109:5×108 | C. | 1:20:1010:109 | D. | 1:10:1010:109 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com