
| A、AgNO3 |
| B、NaCl |
| C、CuCl2 |
| D、Na2SO4 |


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:
| A | ①能使溴的四氯化碳溶液褪色; ②比例模型为 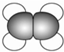 ③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成. ②球棍模型为 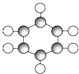 |
| C | ①由C、H、O三种元素组成; ②能与Na反应; ③与E反应生成相对分子质量为88的酯 |
| D | ①相对分子质量比C多18.5; ②在不同条件下,D能生成A,也能生成C |
| E | ①由C、H、O三种元素组成; ②其水溶液能使紫色石蕊试液变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不可通过核磁共振氢谱鉴别苯酚和环己醇 |
| B、淀粉、油脂、蛋白质都能水解,但水解产物不同 |
| C、煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |
| D、米饭在嘴中越咀嚼越甜的原因是淀粉水解生成甜味物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+ Fe3+ Cl- I- |
| B、Ca2+、K+、Cl-、HCO3- |
| C、Mg2+ Na+ SO42-Cl- |
| D、K+ Na+ SO42-NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡后水蒸气的体积分数与H2相等 |
| B、平衡后水的转化率为50% |
| C、平衡后CO体积与CO2相等 |
| D、平衡后CO2的体积分数为20% |
查看答案和解析>>
科目:高中化学 来源: 题型:
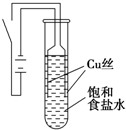 某课外兴趣小组进行电解原理的实验探究,做了如下的实验:以铜为电极,按如图所示的装置电解饱和食盐水.
某课外兴趣小组进行电解原理的实验探究,做了如下的实验:以铜为电极,按如图所示的装置电解饱和食盐水.| 物质 | 氯化铜 | 氧化亚铜 | 氢氧化亚铜(不稳定) | 氯化亚铜 |
| 颜色 | 固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 | 红色 | 橙黄色 | 白色 |
| A、反应结束后最终溶液呈碱性 |
| B、阴极上发生的电极反应为:2H2O+2e?═H2↑+2OH? |
| C、电解过程中氯离子移向阳极 |
| D、试管底部红色的固体具有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、P、Q、R、S的浓度相等 |
| B、P、Q、R、S在容器中共存 |
| C、P、Q、R、S的浓度不再变化 |
| D、P、Q的反应速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、根据物质能否溶于水,将物质分为易溶物质和难溶物质 |
| B、根据化学反应中是否有单质生成把化学反应分为氧化还原反应和非氧化还原反应 |
| C、根据物质中是否含碳元素,将物质分为无机物和有机物 |
| D、根据酸中是否含有氧元素,将酸分为无氧酸和含氧酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com