
����Ŀ�����й������ʵ���Ũ�ȱ�����ȷ����
A��0.3 mol��L1��Na2SO4��Һ�к���Na+��![]() �������ʵ���Ϊ0.9 mol
�������ʵ���Ϊ0.9 mol
B����1 Lˮ����22.4 L����ʱ���ð�ˮ��Ũ�Ȳ���1 mol��L1��ֻ�е�22.4 L��������ˮ�Ƶ�1 L��ˮʱ����Ũ�Ȳ���1 mol��L1
C����K2SO4��NaCl�����Ի��ˮ��Һ�У����Na+��![]() �����ʵ�����ȣ���K+��Cl�����ʵ���Ũ��һ�����
�����ʵ�����ȣ���K+��Cl�����ʵ���Ũ��һ�����
D��10 ��ʱ��0.35 mol��L1��KCl������Һ100 mL������5 gˮ����ȴ��10 ��ʱ�������С��100 mL���������ʵ���Ũ����Ϊ0.35 mol��L1
���𰸡�D
��������A�û��ָ����Һ�����������Һ��Na+��![]() �������ʵ�����һ������0.9 mol��B���Ȼǿ���˰�ˮ�����Ϊ1 L���������ܼ�Ϊ1 L������û��ָ��22.4 L�ǰ����ڱ�״���µ���������������ʵ�����һ����1 mol�����Ƴ�1 L��Һʱ��Ũ��Ҳ��һ����1 mol��L1��C���Na+��
�������ʵ�����һ������0.9 mol��B���Ȼǿ���˰�ˮ�����Ϊ1 L���������ܼ�Ϊ1 L������û��ָ��22.4 L�ǰ����ڱ�״���µ���������������ʵ�����һ����1 mol�����Ƴ�1 L��Һʱ��Ũ��Ҳ��һ����1 mol��L1��C���Na+��![]() �����ʵ������ʱ�����ݻ�ѧʽ��K+��
�����ʵ������ʱ�����ݻ�ѧʽ��K+��![]() ��Na+��Cl�ı�����ϵ���ɵ�c(K+)��c(Cl)=2��1��D�����10 ��ʱ0.35 mol��L1��KCl������Һ��������ˮ�ֺ�����KCl���壬�¶Ȼָ���10 ��ʱ����Ϊ������Һ����Ũ�Ȳ��䡣
��Na+��Cl�ı�����ϵ���ɵ�c(K+)��c(Cl)=2��1��D�����10 ��ʱ0.35 mol��L1��KCl������Һ��������ˮ�ֺ�����KCl���壬�¶Ȼָ���10 ��ʱ����Ϊ������Һ����Ũ�Ȳ��䡣


 ѧ���쳵�����ּ��������ҵ�½����������ϵ�д�
ѧ���쳵�����ּ��������ҵ�½����������ϵ�д� �����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д� Сѧ�����ҵ���ϴ�ѧ������ϵ�д�
Сѧ�����ҵ���ϴ�ѧ������ϵ�д� ���Ž�����ٰθ��νӹ㶫���������ϵ�д�
���Ž�����ٰθ��νӹ㶫���������ϵ�д� �����������ҵ�������������ϵ�д�
�����������ҵ�������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӳ�ʳƷ�����ڵķ����У���ԭ��������������ͬ����
A. ��ʳ������ B. ����� C. �䵪�� D. ʹ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ԡ����ʵ�����Ϊ���ĵļ����ǻ�ѧ����Ļ����������롰���ʵ�������صļ�����ȷ����
A������CO��CO2��O3�������壬���Ƿֱ���1 mol O����������������ʵ���֮��Ϊ3��2��1
B��n g Cl2����m��Clԭ�ӣ����ӵ�����NA����ֵ�ɱ�ʾΪ![]()
C����״���£�11.2 L X������ӵ�����Ϊ16 g����X�����Ħ��������32
D��5.6 g CO��22.4 L CO2�к��е�̼ԭ����һ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷Ͼ�п��Ƥ�Ʊ�����Fe3O4�������Ӽ�������ZnO��һ���Ʊ�����ͼ���£�

��֪��Ksp[Zn(OH)2]= 1.2��10��17��Zn(OH)2��������ǿ�ᣬ��������ǿ��������ڰ�ˮ������[Zn��NH3)4]2����
��1����ҺA�м�ϡH2SO4����Zn(OH)2�����ӷ���ʽΪ_________��
��2�������£�Zn(OH)2������Һ��c(Zn2��)=3��10��6mol/L������ҺA�м���ϡH2SO4���������ܽ������Zn(OH)2��Zn(OH)2��ʼ�ܽ��pHΪ_________��Ϊ��ֹZn(OH)2�ܽ⣬�ɽ�ϡH2SO4��Ϊ_________����lg2=0.3��
��3���������������Σ�NaClO3����ԭΪCl������ԭ������������Ӧ�����ʵ���֮����_________��
��4��������ҺB�Ƶ�Fe3O4�������ӵĹ�����ͨ��N2��ԭ����_________��
��Fe3O4�������ӵ�ֱ���ķ�Χ��_________��
��ȷ����ҺB�к���Fe2�����Լ���_________��
��5���Խ�����ʵ���Ҳ������ÿ�����п���백ˮ��Ӧ�Ʊ�������п��ԭ��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼������Al4C3������ұ�������������ֵ����ڸ�����ֱ�ӻ������Ʊ������д�����������AlN��������Al2O3��
��֪����AlN+NaOH+H2O=NaAlO2+NH3����
��Al4C3��ˮ�Ӵ�����ܿ�ų���ȼ������飬����������������
Ϊ�ⶨijAl4C3��Ʒ�ĺ������������ʵ�鷽����ȡһ��������Ʒ��ѡ������װ�òⶨ��Ʒ��Al4C3�Ĵ��ȣ��г���������ȥ����

��1��д��Al4C3���������������Һ��Ӧ�Ļ�ѧ����ʽ_________.
��2���ⶨ��Ʒ��Al4C3�Ĵ��ȿ���ѡ����ͼװ���е�A��_________��C��
��3���������ʵ�鲽�裺��װ��ʵ��װ�ã�����_________���ټ���ʵ��ҩƷ����������ʵ������Ǵ�Һ©���������μ�NaOHŨ��Һ�����ٲ������壮Ȼ��رշ�Һ©���������ָ������º����µ���������ʹ����Һ����ƽ��Ȼ�������
��4����Ҫѡ��װ��D����Dװ������װ�Լ���_________��������_________��װ�������θ���ܵ�������_________��
��5��Ϊ�ⶨ������������������װ���е�XҺ�������_________������ĸ����
A��CCl4 B��H2O C��![]()
��6��������Ʒ�к���Ԫ�ص�������13.5g���μ�100mL����������Һ����Ʒ��ȫ�ܽ�����������Ҳǡ����ȫ��Ӧ������������������Һ�����ʵ���Ũ��Ϊ_________�������Է�Ӧǰ����Һ����ı仯��
������a�������õ��ɼм�ס������������ͬ�ϣ���Ʒ��ȫ��Ӧ���������ղⶨ�Ľ��_________�����ƫ����ƫС������Ӱ�족��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ȱ���Ⱦ�ϡ�ҽҩ��ҵ���й㷺��Ӧ�ã�ijʵ��С����������װ�úϳ��ȱ���֧���õ�����̨����ʡ�ԣ���ͨ��һ�������ᴿ�ȱ���
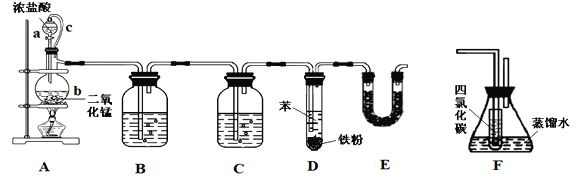
��Ӧ��Ͳ������������б����£�
�ܶ�/g��cm��3 | �е�/�� | ˮ���ܽ��� | |
�� | 0.879 | 80.1 | �� |
�ȱ� | 1.11 | 131.7 | ���� |
�밴Ҫ��ش��������⡣
��1��װ��A����c��������______________��װ��E��������__________________��
��2��ʵ��ʱ��ʹa�е�Ũ���Ỻ�����£��ɹ۲쵽����b�ڵ�������________________��д����Ӧ�����ӷ���ʽ______________________________________��
��3��Ϊ֤�������ͱ���������ȡ�������Ǽӳɷ�Ӧ����С����װ��F˵������װ��F����________֮�䣨����ĸ����F��С�Թ���CCl4��������___________________������ʹ�õ��Լ���______________��
��4����֪D�м���5 mL���������ᴿ���ռ����ȱ�3.0 g�����ȱ��IJ���Ϊ_________%��������λ��Ч���֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��������ؾ���(KO2)��������ṹ����ͼΪ�������ؾ����һ����������������С���ظ���Ԫ�������й�����˵����ȷ���ǣ� �� ��

A. KO2��ֻ�������Ӽ�
B. �����У�����ԭ��֮�䶼�������Ӽ����
C. ��������ÿ��K+���������O2-��6��
D. �������ػ�ѧʽΪKO2��ÿ����������1��K+��1��O2-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����칬һ�š��Ĺ���ϵͳ������������ȼ�ϵ�أ�RFC����RFC��һ�ֽ�̫���ܵ�ص��ˮ����������ȼ�ϵ�ؼ������ϵĿɳ���ء���ͼΪRFC����ԭ��ʾ��ͼ����ĤΪ����ѡ������Ĥ��������˵������ȷ����
![]()

װ��I װ��II
A. c���Ϸ����ĵ缫��Ӧ�ǣ�O2 + 4H+ + 4e- = 2H2O
B. ����0.1mol����ת��ʱ��b������1.12L ����Y����״���£�
C. װ��I��װ��II�ĵ������Һ�У��������˶������෴
D. RFCϵͳ����������ֻ����3����ʽ������ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�ˮ��Һ�ܵ��磬���䱾�����ڷǵ���ʵ���(����)
A. CH3COOHB. �ɱ�C. �ƾ�D. Cl2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com