
| A. | SO2 | B. | CO | C. | N2 | D. | NO2 |
分析 空气日报的检测项目是:氮氧化物、二氧化硫、一氧化碳、悬浮颗粒物等空气的污染物,据此分析判断即可.
解答 解:空气质量日报中的项目是空气的主要污染物,空气的污染物主要包括:氮氧化物、二氧化硫、一氧化碳、悬浮颗粒物等.
A.SO2属于空气污染物,故A正确;
B.CO属于空气污染物,故B正确;
C.N2是空气的成分,不属于空气污染物,故C错误;
D.NO2属于空气污染物,故D正确.
故选C.
点评 本题考查环境污染知识,能源、信息、材料、环境是当今世界四大首要问题,特别是环保问题,现已经引起了全球的高度重视,是高考的热点问题,主要考查温室效应、空气质量日报、空气污染来源、空气污染的防治等,题目难度不大.


 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案科目:高中化学 来源: 题型:解答题
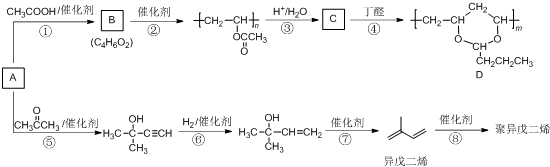
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
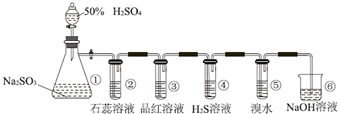
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加5 mL水,c (H+)增大 | B. | 加少量NaCl固体,c (H+)不变 | ||
| C. | 加少量碳酸钙粉末,c(HClO)升高 | D. | 加少量Na2SO3固体,溶液pH升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 决定化学反应速率的主要因素是参加反应的物质的性质 | |
| B. | 升高温度可使吸热反应的反应速率增大,使放热反应的反应速率减小 | |
| C. | 对于有气体参加的反应,增大压强,反应速率加快 | |
| D. | 催化剂能增大单位体积内活化分子的百分数,从而增大化学反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
已知:  | |
步骤: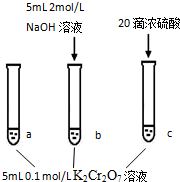 | 现象: 待试管b中颜色不变后与试管a比较,溶液颜色变浅. 滴加浓硫酸,试管c温度略有升高,溶液颜色与试管a相比,变深. |
| A. | 该反应是一个氧化还原反应 | |
| B. | 待试管b中溶液颜色不变的目的是使Cr2O72-完全反应 | |
| C. | 该实验不能证明减小生成物浓度,平衡正向移动 | |
| D. | 试管c中的现象说明影响平衡的主要因素是温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
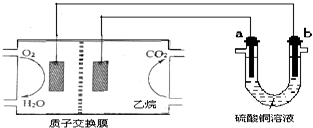
| A. | 燃料电池工作时,正极反应为O2+2H2O+4e-═4OH- | |
| B. | a极是铜,b极是铁时,硫酸铜溶液浓度减小 | |
| C. | a、b两极若是石墨,在同温同压下a极产生的气体与电池中消耗的乙烷体积的7/2 | |
| D. | a极是纯铜,b极是粗铜时,a极上有铜析出,b极逐渐溶解,两极质量变化相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com