
【题目】利用下图装置可以进行实验并能达到实验目的的是
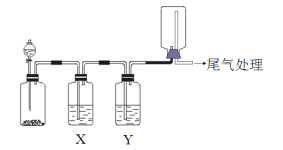
选项 | 实验目的 | X中试剂 | Y中试剂 |
A | 用MnO2和浓盐酸制取并收集纯净干燥的Cl2 | 饱和食盐水 | 浓硫酸 |
B | 用Cu与稀硝酸制取并收集纯净干燥的NO | 水 | 浓硫酸 |
C | 用CaCO3和稀盐酸制取并收集纯净干燥的CO2 | 饱和NaHCO3溶液 | 浓硫酸 |
D | 验证电石与饱和食盐水反应生成的气体的性质并收集 | CuSO4溶液 | KMnO4溶液 |
A. A B. B C. C D. D
 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】起始时向密闭容器中充入amolNO2(g),反应 2NO2(g)![]() N2O4(g)达到平衡后,再向容器内通bmolNO2(g),又达到平衡时,下列说法中不正确的是( )
N2O4(g)达到平衡后,再向容器内通bmolNO2(g),又达到平衡时,下列说法中不正确的是( )
A. 恒温恒压和恒温恒容条件下,NO2 的物质的量都增大
B. 恒温恒压和恒温恒容条件下,NO2 的物质的量浓度都增大
C. 恒温恒压和恒温恒容条件下,NO2 转化率前者不变,后者增大
D. 恒温恒压和恒温恒容条件下,混合气体的平均摩尔质量前者不变,后者增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于某些离子的检验及结论一定正确的是
A. 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO![]()
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO![]()
C. 加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有NH![]()
D. 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲从Fe3+、Al3+的混合液中分离并测定Fe3+的浓度,实验方案如下:

已知:①乙醚[(C2H5)2O]:沸点34.5℃,微溶于水,易燃。
②盐酸浓度较高时,Fe3+与HCl、乙醚形成化合物[(C2H5)2OH][FeCl4]溶于乙醚;当盐酸浓度降低时,该化合物解离。
(1)操作I的名称是_______。
(2)检验溶液Y中是否残留Fe3+的实验方法是_________ 。
(3)蒸馏装置如下图所示,该装置图中存在的错误是________。

(4)滴定前,加入的适量溶液Z是_______(填序号)。
A.H2SO4~H3PO4 B.H2SO3~H3PO4 C.HNO3~H3PO4 D.HI~H3PO4
(5)滴定达到终点时,消耗0.1000mol/LK2Cr2O7溶液5.00mL。根据该实验数据,起始所取的试样Fe3+、Al3+的混合液中c(Fe3+)为______。
(6)上述测定结果存在一定的误差,为提高该滴定结果的精密度和准确度,可采取的措施是_______。
A.稀释被测试样 B.增加平行测定次数
C.减少被测试样取量 D.降低滴定剂浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】飘尘是物质燃烧时产生的粒状漂浮物,颗粒很小,不易沉降,它与空气中的SO2和O2接触时,SO2会部分转化为SO3,使空气的酸度增加,飘尘所起的作用可能是
A. 氧化剂 B. 还原剂 C. 催化剂 D. 载体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过简单的计算完成下列问题:
(1)已知:常温下HF的Ka=1×10-4,NH3H2O的Kb=1×10-5,则NH4F溶液显_______性,保存此溶液应该放在_______中。
(2)已知:常温下 H2S的Ka1=1×10-7、Ka2=1×10-15,CuS的Ksp=1×10-36,FeS的Ksp=1×10-17,则:
①反应CuS(s)+2HCl(aq)![]() H2S(aq)+CuCl2(aq)的K=__________;反应FeS(s)+2HCl(aq)
H2S(aq)+CuCl2(aq)的K=__________;反应FeS(s)+2HCl(aq)![]() H2S(aq)+FeCl2(aq)的 K=_____;
H2S(aq)+FeCl2(aq)的 K=_____;
由计算结果我们可以知道CuS和FeS中________可溶于盐酸。
②反应 CuS(s)+Fe2+(aq)![]() FeS(s)+Cu2+(aq)的K=_____;除去废水中的 Cu2+使用过量的FeS固体的优点有:a.可以除去废水中的Cu2+,过量的FeS和生成的CuS可以通过过滤一并除去;b. _________________________________。
FeS(s)+Cu2+(aq)的K=_____;除去废水中的 Cu2+使用过量的FeS固体的优点有:a.可以除去废水中的Cu2+,过量的FeS和生成的CuS可以通过过滤一并除去;b. _________________________________。
(3)已知:常温下 Fe(OH)3的 Ksp=1×10-38,则 Fe3+沉淀完全的pH=______;配置FeCl3溶液的方法是______。(以浓度≤10-5mol/L为沉淀完全)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铁、铝的混合物进行如下实验:

(1)操作X的名称是___________。
(2)气体A是___________。
(3)加入足量NaOH 溶液时发生反应的离子方程式为______________;加入盐酸发生反应的离子方程式为_______________。
(4)溶液B 中阴离子除OH-外还有_________,溶液D中存在的金属离子为___________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com