
【题目】起始时向密闭容器中充入amolNO2(g),反应 2NO2(g)![]() N2O4(g)达到平衡后,再向容器内通bmolNO2(g),又达到平衡时,下列说法中不正确的是( )
N2O4(g)达到平衡后,再向容器内通bmolNO2(g),又达到平衡时,下列说法中不正确的是( )
A. 恒温恒压和恒温恒容条件下,NO2 的物质的量都增大
B. 恒温恒压和恒温恒容条件下,NO2 的物质的量浓度都增大
C. 恒温恒压和恒温恒容条件下,NO2 转化率前者不变,后者增大
D. 恒温恒压和恒温恒容条件下,混合气体的平均摩尔质量前者不变,后者增大
【答案】B
【解析】应将b mol NO2气体建立和a mol NO2相同条件下的等效平衡,恒温恒压条件,相当于两容器相加,平衡不移动;恒温恒容条件,相当于原体系容器增大压强,平衡向正向移动。A、无论恒温恒压和恒温恒容条件下,增加NO2的量,增加的NO2都不能反应完,则NO2 的物质的量都增大,选项A正确;B、恒温恒压条件下,增加NO2的量,反应按比例转化,故NO2 的物质的量浓度不变,选项B不正确;C、恒温恒压条件下,反应按比例进行,NO2 转化率不变,恒温恒容条件下,增加NO2的量相当于增大压强平衡向气体体积缩小的方向移动,则NO2 转化率增大,选项C正确;D、恒温恒压条件下,反应按比例进行,混合气体的平均摩尔质量不变,恒温恒容条件下,增加NO2的量相当于增大压强平衡向气体体积缩小的方向移动,气体总物质的量减小,混合气体的平均摩尔质量增大,选项D正确。答案选B。


科目:高中化学 来源: 题型:
【题目】氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作。

回答下列问题:
(1)检验滤液中的![]() 的方法是____________。
的方法是____________。
(2)试剂I的化学式为__________,加入试剂I后,①对应的实验操作是____,①中发生反应的离子方程式为__________。
(3)试剂II的化学式为_________,②中加入试剂II的目的是______。
(4)试剂III的名称是________,③中发生反应的离子方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,A、B、C的起始浓度分别是0.5mol/L、0.1 mol/L、1.6mol/L,可逆反应A(g)+B(g)![]() 2C(g)达到平衡时,下列数据合理的是
2C(g)达到平衡时,下列数据合理的是
A. c(A)=1.0mol/L c(B)=0.2mol/L B. c(B)=0.5mol/L c(C)=1.2mol/L
C. c(A)=0.4mol/L c(C)=1.8mol/L D. c(A )=0.9mol/L c(B)=0.5mo/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个容积均为1.0L的恒容密闭容器中发生反应:
CH3OH(g)+CO(g) ![]() CH3COOH(g)△H<0。下列说法正确的是
CH3COOH(g)△H<0。下列说法正确的是
容器编号 | 温度/K | 物质的起始浓度/mol/L | 物质的平衡浓度/mol/L | ||
c(CH3OH) | c(CO) | c(CH3COOH) | c(CH3COOH) | ||
I | 530 | 0.50 | 0.50 | 0 | 0.40 |
II | 530 | 0.20 | 0.20 | 0.40 | |
III | 510 | 0 | 0 | 0.50 | |
A. 达平衡时,容器I与容器II中的总压强之比为3:4
B. 达平衡时,容器II中![]() 比容器I中的大
比容器I中的大
C. 达平衡时,容器Ⅲ中的正反应速率比容器I中的大
D. 达平衡时,容器I中CH3OH转化率与容器III中CH3COOH转化率之和小于1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯碱(Na2CO3)在生产生活中具有广泛的用途。
Ⅰ.以下是实验室模拟制碱原理制取Na2CO3的流程图。
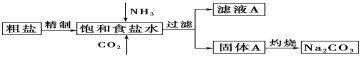
下表是四种物质在100g水中不同温度的溶解度

(1)粗盐中含有的杂质离子有Ca2+、Mg2+、SO42-等。精制除杂的步骤顺序是a→________→________→________→b(填字母编号)。
a.粗盐溶解,滤去沉渣 b.加入盐酸调pH c.加入Ba(OH)2溶液
d.加入Na2CO3溶液 e.过滤
(2)向饱和食盐水中先通入_______,后通入________,生成固体A的化学方程式为____
Ⅱ.制得的碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案.请回答下列有关问题:
方案一:把6g样品溶解后加入过量的CaCl2溶液,将所得沉淀过滤、洗涤、烘干后得到5g固体。
(3)洗涤沉淀的具体操作是_____________________________。
(4)根据实验中测得的有关数据,计算纯碱样品Na2CO3的质量分数为___________(结果保留小数点后一位)。
方案二:利用下图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去)。
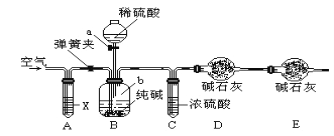
已知:碱石灰为氢氧化钠和氧化钙的混合物。
(5)实验开始前应进行的操作是______________________________。
(6)仪器a的名称为___________________,装置A中试剂X应选用_________________。
(7)装置E的作用是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列5种有机物:①2-甲基丙烷;②乙醇;③丙烷;④丁烷;⑤苯酚。按它们的沸点由高到低的顺序排列正确的是( )
A. ①②③④⑤ B. ⑤②④①③ C. ⑤④②①③ D. ③①②⑤④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下 0.1mol/L 氨水pH为11,则下列说法中不正确的是( )
A. 此溶液中 NH3H2O 在常温下的电离度约为1%
B. 若向此溶液中通入少量氨气,NH3H2O电离平衡正向移动,水的电离平衡逆向移动
C. 若向其中加入 pH为11的NaOH溶液,NH3H2O电离平衡不移动,但n(NH4+)减小
D. 若向其中加入少量水,溶液中n(H+)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置可以进行实验并能达到实验目的的是
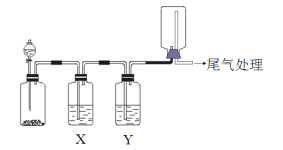
选项 | 实验目的 | X中试剂 | Y中试剂 |
A | 用MnO2和浓盐酸制取并收集纯净干燥的Cl2 | 饱和食盐水 | 浓硫酸 |
B | 用Cu与稀硝酸制取并收集纯净干燥的NO | 水 | 浓硫酸 |
C | 用CaCO3和稀盐酸制取并收集纯净干燥的CO2 | 饱和NaHCO3溶液 | 浓硫酸 |
D | 验证电石与饱和食盐水反应生成的气体的性质并收集 | CuSO4溶液 | KMnO4溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下列装置进行有关Cl2的实验。下列说法不正确的是


A. Ⅰ图中:实验现象证明氯气无漂白作用,氯水有漂白作用
B. Ⅱ图中:闻Cl2的气味
C. Ⅲ图中:生成棕黄色的烟
D. Ⅳ图中:若气球干瘪,证明Cl2可与NaOH反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com