
| X | Y | ||
| Z | W |
| A. | X位于元素周期表中第2周期、第ⅤA族 | |
| B. | Y的一种氢化物不稳定,易分解 | |
| C. | W的非金属性比Y的非金属性弱 | |
| D. | Z的最高价氧化物的水化物可与X的最高价氧化物的水化物反应 |
分析 由X、Y、Z、W四种短周期元素的位置可知,X、Y在第二周期,Z、W在第三周期,设X的原子序数为x,则W的原子序数为x+9,X、W的质子数之和为21,则x+x+9=21,解得x=6,所以X为C元素,可推知Z为Al、Y为O、W为P,然后结合元素及其单质、化合物的性质来解答.
解答 解:由X、Y、Z、W四种短周期元素的位置可知,X、Y在第二周期,Z、W在第三周期,设X的原子序数为x,则W的原子序数为x+9,X、W的质子数之和为21,则x+x+9=21,解得x=6,所以X为C元素,可推知Z为Al、Y为O、W为P.
A.X为碳元素,位于元素周期表中第2周期第ⅣA族,故A错误;
B.Y的氢化物中,H2O2不稳定,易分解,故B正确;
C.W的非金属性比Y的强,故C错误;
D.Z的最高价氧化物的水化物为氢氧化铝,X的最高价氧化物的水化物为碳酸,氢氧化铝不能与碳酸反应,故D错误,
故选B.
点评 本题考查位置结构性质关系综合应用,明确短周期及原子序数的关系来推断各元素是解题的关键,注意理解同主族元素原子序数关系,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 强电解质一定易溶于水 | |
| B. | 常温下,强酸和弱酸的浓度相同时,强酸中水的电离程度比弱酸的水的电离程度小 | |
| C. | 对可逆反应,升高温度一定存在v(正)>v(逆) | |
| D. | 钢铁在海水中发生电化腐蚀时,铁是正极被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化合物 | 燃烧热/kJ•mol-1 | 化合物 | 燃烧热/kJ•mol-1 |
| 甲烷 | 891.0 | 正丁烷 | 2878.0 |
| 乙烷 | 1560.8 | 异丁烷 | 2869.6 |
| 丙烷 | 2221.5 | 异戊烷 | 3531.3 |
| A. | 正戊烷的燃烧热小于3531.3kJ•mol-1 | |
| B. | 稳定性:正丁烷>异丁烷 | |
| C. | 乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g);△H=-1560.8 kJ | |
| D. | 相同物质的量的烷烃CnH2n+2,n越大,燃烧放出的热量越多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
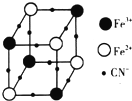 过渡金属元素及其化合物在合金材料以及催化剂等方面应用非常广泛.
过渡金属元素及其化合物在合金材料以及催化剂等方面应用非常广泛.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O在高温下难分解,而H2S在300℃时就分解,说明O非金属性比S强 | |
| B. | H2CO3的酸性比HClO的酸性强,所以C的非金属性比Cl强 | |
| C. | NaOH的碱性比Mg(OH)2的碱性强,所以Na的金属性比Mg强 | |
| D. | Fe3+的氧化性比Cu2+的氧化性强,但Fe的金属性比Cu强 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北石家庄辛集中学高二上阶段考一化学卷(解析版) 题型:实验题
某化学课外小组查阅资料得知:苯和液溴在有溴化铁(FeBr3)存在的条件下可发生反应生成溴苯和溴化氢,此反应为放热反应。他们设计了下图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A中。如图是制取溴苯的装置。试回答:
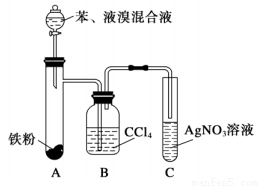
(1)装置A中发生反应的化学方程式是______________________。
(2)装置C中看到的现象是______________,证明________________。
(3)装置B是吸收瓶,内盛CCl4液体。如果没有B装置而将A、C直接相连,你认为是否妥当?__________(填“是”或“否”),理由是_____________________。
(4)实验完毕后将A试管中的液体倒在装有冷水的烧杯中,烧杯_________(填“上”或“下”)层为溴苯,这说明溴苯___________且_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若X为单质铝,则Y的气体产物只能是氢气 | |
| B. | 若X为NaHCO3,则Z一定有CO2 | |
| C. | 若Y、Z为含铝元素的两种盐,则X一定为Al(OH)3 | |
| D. | 若X为乙酸乙酯,则生成物Y、Z中均含有乙醇 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北石家庄辛集中学高二上阶段考一化学卷(解析版) 题型:选择题
下列关于烷烃性质的叙述中,不正确的是( )
A.烷烃同系物随着相对分子质量增大,熔点、沸点逐渐升高
B.烷烃都能使溴水、酸性KMnO4溶液褪色
C.烷烃跟卤素单质在光照条件下能发生取代反应
D.烷烃同系物的密度随着相对分子质量的增大逐渐增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com