
【题目】依据氧化还原反应:2Ag+(aq) + Cu(s)Cu2+(aq) + 2Ag(s)设计的原电池如图所示。
请回答下列问题:
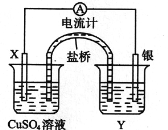
(1)电极X的材料是____________________;电解质溶液Y是____________;
(2)银电极为电池的___________极,发生的电极反应为_____________________;X电极上发生的电极反应为_____________________。
(3)外电路中的电子是从___________电极流向___________电极。
科目:高中化学 来源: 题型:
【题目】下列图示的四种实验操作名称从左到右依次是( ) 
A.过滤、蒸发、蒸馏、分液
B.过滤、蒸馏、蒸发、分液
C.蒸发、蒸馏、过滤、分液
D.分液、蒸馏、蒸发、过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“84”消毒夜在日常生活中被广泛使用。该消毒液无色,pH大于7,对某些有色物质有漂白作用。你认为它可能的有效成分是( )
A. SO2 B. Na2CO3 C. KMnO4 D. NaClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】AlN广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应Al2O3+N2+3C![]() 2AlN+3CO合成。下列叙述正确的是( )
2AlN+3CO合成。下列叙述正确的是( )
A. AlN为氧化产物
B. AlN的摩尔质量为41g
C. 上述反应中,每生成1molAlN需转移3mol电子
D. 上述反应中,N2是还原剂,Al2O3是氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在周期表中的相对位置如图所示,其中W元素的原子结构示意图为 ![]() .请回答下列问题:
.请回答下列问题:
W | X | Y |
Z |
(1)Z元素位于元素周期表中第周期族.
(2)X元素的最简单气态氢化物能与其最高价氧化物对应的水化物反应,得到的化合物属于(填“离子化合物”或“共价化合物”).
(3)X、Y、Z三种元素的原子半径由大到小的顺序为(用元素符号表示).
(4)写出W单质与X的最高价氧化物对应水化物的浓溶液反应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列微粒半径大小比较错误的是( )。
A. K>Na>Li B. Na+>Mg2+>Al3+
C. Mg2+>Na+>F- D. Cl->F->F
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化学知识在生活中应用广泛。下列说法不正确的是( )
A.医用酒精的质量分数为75%
B.苯酚有毒,不小心沾到皮肤上,应用酒精清洗
C.甘油加水做护肤剂
D.福尔马林是甲醛的水溶液,具有杀菌防腐能力,不可用于保鲜鱼、肉等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】充分利用黄铁矿(主要成份为FeS2)对资源和环境具有重要的意义。
(1)一种酸性条件下催化氧化黄铁矿的物质转化关系如下面图Ⅰ所示。
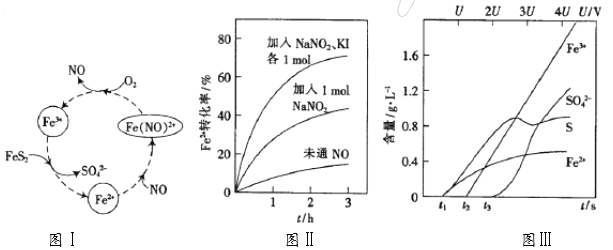
①图Ⅰ中,NO起的是_____作用;O2氧化FeS2生成Fe3+的离子方程式为____________;
②硝酸也可以将FeS2氧化为Fe3+和SO42-,但使用稀硝酸比浓硝酸的反应速率快很多,其原因是:_________。
(2)控制Fe3+的浓度、溶液体积和通入O2的速率一定,图Ⅱ表示当改变其它条件时Fe2+被氧化的转化率随时间的变化。
①加入NaNO2发生反应:3NO2-+2H+==NO3-+2NO↑+H2O。若3molNaNO2完全反应,则转移的电子数为____________________mol。
②在酸性溶液中,加入NaNO2、KI发生反应生成NO和I2,该离子反应方程式为______ ;图Ⅱ中曲线从下至上, Fe2+转化速率依次增大的原因是________。
(3)为研究FeS2作电极时的放电规律,以FeS2作阳极进行电解,由FeS2放电产生的粒子的含量与时间(t)、电压(U)之间的关系如图Ⅲ所示。
①t1至t2间FeS2发生的电极反应式为_________________。
②当电压值介于3.5U~4.4U之间时,FeS2放电所得的主要粒子为_______________。
③黄铁矿含有杂质钴和镍。若电解一段时间,c(Fe3+)=1×10-2mol·L-1时,通过计算判断:pH控制为_______不会产生Fe(OH)3沉淀;当使Co2+沉淀完全时,Fe3+_____(填:“已经”或“没有”)开始沉淀。{已知:离子浓度≤1×10–5mol·L–1认为沉淀完全;Ksp[Fe(OH)3]=3.8×10–38、Ksp[Co(OH)2]=2×10–15, ![]() = – 0.16}
= – 0.16}
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com