
在4 ℃时向100 mL水中溶解了22.4 L 氯化氢气体(标准状况下测得)后形成的溶液。下列说法中正确的是
A.该溶液物质的量浓度为 10 mol/L
B.该溶液物质的量浓度因溶液的密度未知而无法求得
C.该溶液溶质的质量分数因溶液的密度未知而无法求得
D.所得溶液的体积为 22.5 L
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
| T/℃ | 700 | 800 | 850 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| 时间/min | CO2 | H2 | CO | H2O |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
| (0.100)2 |
| 0.100×0.200 |
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
| (0.100)2 |
| 0.100×0.200 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
| ||
| ||
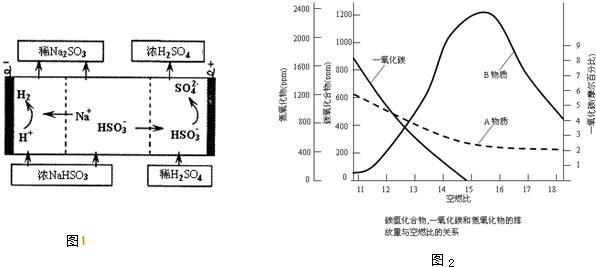
查看答案和解析>>
科目:高中化学 来源:2007新课标高一化学同步测试 第二节 化学计量在实验中的应用(B) 题型:013
|
在4 ℃时向100 mL水中溶解了22.4 L HCl气体(标准状况下测得)后形成的溶液.下列说法中正确的是 | |
| [ ] | |
A. |
该溶液物质的量浓度为10 mol·L-1 |
B. |
该溶液物质的量浓度因溶液的密度未知而无法求得 |
C. |
该溶液中溶质的质量分数因溶液的密度未知而无法求得 |
D. |
所得溶液的体积为22.5 L |
查看答案和解析>>
科目:高中化学 来源:广东省普通高中2009年高中学业水平考试统一模拟测练试题(会考)(化学科) 题型:021
|
在4℃时向100 mL水中溶解了22.4 L HCl气体(标准状况下测得)后形成的溶液.下列说法中不正确的是 | |
A. |
该溶液物质的量浓度为10 mol·L-1 |
B. |
该溶液物质的量浓度因溶液的密度未知而无法求得 |
C. |
该溶液中溶质的质量分数因溶液的密度未知而无法求得 |
D. |
所得溶液的体积为22.5 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com