
【题目】工业中很多重要的原料都是来源于石油化工,回答下列问题
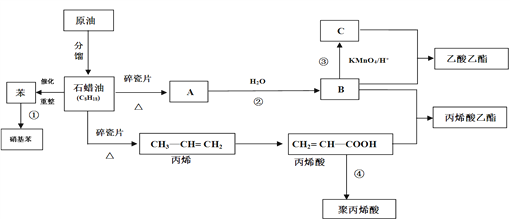 (1)A的结构简式为________。
(1)A的结构简式为________。
(2)丙烯酸中含氧官能团的名称为_____________。
(3)①③反应的反应类型分别为_____________、________________。
(4)写出下列反应方程式
① 反应②的方程式_____________________;
② 反应④的方程式_________________________________________;
③ 丙烯酸 + B![]() 丙烯酸乙酯_____________________。
丙烯酸乙酯_____________________。
(5)丙烯酸(CH2 = CH — COOH)的性质可能有(_______)
① 加成反应 ②取代反应 ③加聚反应 ④中和反应 ⑤氧化反应
A.只有①③ B.只有①③④
C.只有①③④⑤ D.①②③④⑤
(6)丙烯分子中,最多有_________个原子共面。
【答案】 CH2 = CH2 羧基 取代反应 氧化反应 CH2 = CH2 + H2O ![]() CH3CH2OH
CH3CH2OH  CH2= CH—COOH + CH3CH2OH
CH2= CH—COOH + CH3CH2OH ![]() CH2 = CH—COOC2H5 + H2O D 7
CH2 = CH—COOC2H5 + H2O D 7
【解析】由转化关系中,B氧化生成C,且二者反应生成乙酸乙酯,则B为乙醇,C为乙酸,而A与发生反应得到乙醇,应是乙烯与水发生加成反应,故A为乙烯,乙醇与丙烯酸发生酯化反应生成丙烯酸乙酯,丙烯酸发生加聚反生成聚丙烯酸,苯与浓硝酸在浓硫酸作催化剂、加热条件下发生取代反应生成硝基苯,
(1)A为乙烯,含有碳碳双键,结构简式为CH2=CH2。
(2)丙烯酸中含氧官能团的名称为:羧基。
(3)反应①是苯发生硝化反应,属于取代反应,反应③是乙醇发生氧化反应生成乙酸,属于氧化反应。
(4)写出下列反应方程式
① 反应②是乙烯与水反应生成乙醇,方程式:CH2 = CH2 + H2O ![]() CH3CH2OH ;
CH3CH2OH ;
② 反应④是丙烯酸发生加聚反应生成聚丙烯酸,方程式: ;
;
③ B 是CH3CH2OH,丙烯酸 + B反应生成丙烯酸乙酯和水,反应方程式为:CH2= CH—COOH + CH3CH2OH ![]() CH2 = CH—COOC2H5 + H2O。
CH2 = CH—COOC2H5 + H2O。
(5)丙烯酸(CH2=CH-COOH)含有碳碳双键,具有烯烃的性质,可以发生加成反应、氧化反应、加聚反应; 含有羧基,具有羧酸的性质,可以发生中和反应、取代反应,故选D。
(6)乙烯中,当有一个H被一个甲基取代后,碳碳双键连接的原子处于碳碳双键的平面内,旋转碳碳单键可以使甲基中的一个H原子处于碳碳双键的平面结构内,故最多有7个原子处于同一平面内,故答案为:7


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】如图是Zn和Cu形成的原电池,回答下列问题:

(1)正极发生____反应(选填“氧化”或“还原”),负极电极反应式为:____。
(2)电子流动方向,从____电极(选填“Cu”或“Zn”),经外电路,流向另一电极。阳离子向____电极定向移动(选填“Cu”或“Zn”)。
(3)有0.1 mol电子流过导线,则产生H2在标准状况下的体积为____,若是断开Zn和Cu之间的导线,产生气泡的速度____(选填“加快”、“不变”或“减慢”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【选修5:有机化学基础】化合物E是一种医药中间体,常用于制备抗凝血药,可以通过下图所示的路线合成:

(1)E中的含氧官能团名称为 。
(2)B转化为C的反应类型是 。
(3)写出D与足量NaOH溶液完全反应的化学方程式 。
(4)1molE最多可与 molH2加成。
(5)写出同时满足下列条件的B的一种同分异构体的结构简式 。
A.苯环上只有两个取代基,且除苯环外无其他环状结构
B.核磁共振氢谱只有4个峰
C.能与FeCl3溶液发生显色反应
(6)已知:酚羟基一般不易直接与羧酸酯化,甲苯可被酸性高锰酸钾溶液氧化为苯甲酸。试参照如下和成路线图示例写出以苯酚、甲苯为原料制取苯甲酸苯酚酯(![]() )的合成路线(无机原料任选)。合成路线流程图示例如下:
)的合成路线(无机原料任选)。合成路线流程图示例如下:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnO2的一些性质或用途如图,下列说法正确的是( )

A. ①、②、③三个反应中MnO2均作氧化剂
B. 足量MnO2与2 L 10 mol/L HCl共热,可生成5 mol Cl2
C. 反应②若生成1 mol Al2O3,则反应过程中转移12 mol电子
D. 反应③中K2CO3和KNO3的化学计量数均为1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫酸镁和硫酸铝的混合溶液中,c(Mg2+ )=2 mol·L-1,c(SO42-)=6.5 mol·L-1,若将200 mL此混合液中的Mg2+和Al3+分离,至少应加入1.6 mol·L-1氢氧化钠溶液的体积是
A.0.5 L B.1.625 LC.1.8 LD.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.凡是放热反应都是自发的,由于吸热反应都是非自发的
B.自发反应一定是熵增大,非自发反应一定是熵减少或不变
C.自发反应在恰当条件下才能实现
D.自发反应在任何条件下都能实现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇是一种重要的化工原料,由乙醇为原料衍生出的部分化工产品如下图所示:

(1)A是一种遇到碘单质能变蓝的多糖,A的分子式是_______________。
(2)物质B、C都能在加热条件下与新制的氢氧化铜反应产生砖红色沉淀,但不能发生水解反应,B中官能团的名称为____________,写出反应②的化学方程式___________________。
(3)下图是实验室通过反应①制取少量E的装置图。

实验时,加热前试管a中三种化学试剂的加入顺序依次为__________________(填名称),其中浓硫酸的作用是____________,写出试管a中生成E的化学反应方程式___________________。
(4)上述流程中C2H3Cl的结构简式____________。
(5)上述流程中标号①至④的反应中,与下列反应属同一反应类型的有______________。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂。
(1)常温下,可用铁或者铝制的容器盛放浓硝酸,说明浓硝酸具有_________ 性
A.酸性 B.强氧化性 C.吸水性 D.脱水性
(2)工业上用洗净的废铜屑作原料来制备硫酸铜。下列制备方法符合“绿色化学”思想的是_______________________________(填序号)。
① Cu + H2SO4(浓)![]() CuSO4 ② Cu
CuSO4 ② Cu![]() CuO
CuO![]() uSO4
uSO4
写出①中反应的化学方程式:________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com