
| A. | 铜锌原电池中铜是正极 | |
| B. | 用电解法精炼铜时粗铜作阴极 | |
| C. | 在电解饱和CuCl2溶液时,用铜作阳极 | |
| D. | 电解饱和食盐水时,用铜片作阳极 |
分析 A.铜锌原电池中,锌是负极、铜是正极;
B.用电解法精炼铜时,粗铜作阳极;
C.在电解饱和CuCl2溶液时,用铜作阳极,活性电极失电子发生氧化反应;
D.电解饱和食盐水时,如果阳极是铜,则阳极上铜失电子而不是阴离子失电子.
解答 解:A.铜锌原电池中,锌易失电子发生氧化反应而作负极、铜作正极,故A正确;
B.用电解法精炼铜时,粗铜作阳极、纯铜作阴极,电解质为可溶性铜盐,故B错误;
C.在电解饱和CuCl2溶液时,用铜作阳极,活性电极铜失电子发生氧化反应,应用惰性电极电极饱和氯化铜溶液,故C错误;
D.电解饱和食盐水时,如果阳极是铜,则阳极上铜失电子而不是阴离子失电子,所以阳极上得不到氯气,故D错误;
故选A.
点评 本题考查原电池和电解池原理,知道原电池正负极的判断方法、电解精炼时对电极材料的要求,易错选项是CD,注意:活泼金属作阳极时阳极上失电子的物质,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | SO2使溴水褪色与乙烯使KMnO4溶液褪色的原理相同 | |
| B. | 制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中乙酸 | |
| C. | 用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 | |
| D. | 碳酸氢钠溶液中滴入苯酚的水溶液后不会放出二氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
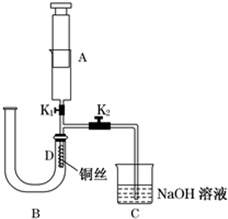
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ②③④ | C. | ①②④ | D. | ②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、OH-、SO42- | B. | Fe3+、K+、Cl-、SCN- | ||
| C. | Na+、K+、CO32-、NO3- | D. | H+、Al3+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 混合物 | 试剂(足量) | 分离方法 |
| A | 苯(苯酚) | 浓溴水 | 过滤 |
| B | 乙烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
| C | 乙酸乙酯(乙酸) | 饱和Na2CO3溶液 | 分液 |
| D | 乙酸(乙醛) | 新制Cu(OH)2悬浊液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com