
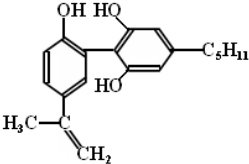
| A. | 该分子中所有碳原子一定都在一个平面上 | |
| B. | 该分子遇FeCl3溶液显紫色,但与苯酚不属于同系物 | |
| C. | 1mol该物质与浓溴水和H2反应时,最多消耗Br2和H2的物质的量分别为4mol、7mol | |
| D. | 滴入酸性KMnO4溶液,观察到紫色褪去,可证明分子中存在双键. |
分析 该有机物含有酚羟基,可与溴水发生取代反应,可与高锰酸钾发生氧化反应,含有C=C官能团,可发生加成、氧化反应,结合苯环、乙烯的结构特征判断有机物的空间结构特点,以此解答该题.
解答 解:A.从苯环的平面结构及乙烯的平面结构出发,把上述结构分成三部分:右边以苯环为中心8个碳原子共平面,左边以苯环为中心8个碳原子共平面,还有以C=C为中心4个碳原子共平面,因C-C可自由旋转,则上述三个平面可以重合,但不一定共平面,故A错误;
B.此有机物遇FeCl3溶液显紫色,苯酚的同系物应符合有且只有一个苯环,且苯环上只连一个羟基,其余全部是烷烃基,故B正确;
C.与浓溴水反应酚类为邻对位上的氢被溴取代,左边苯环邻对位上只有一个H,右边苯环邻对位上有两个H,还有一个C=C与溴水发生加成反应,共消耗4 mol的Br2;两个苯环、一个C=C共消耗7 mol的H2,故C正确;
D.能使酸性KMnO4褪色的官能团有酚羟基、C=C、苯环上的甲基,故D错误.
故选BC.
点评 本题考查的是由有机物结构推断物质性质,首先分析有机物的结构简式,找出官能团,根据有机物官能团的性质进行判断,易错点为A,注意有机物空间结构的分析,题目难度中等.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:选择题
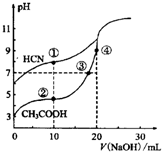
| A. | 点①和点②所示溶液中:c(CH3COO-)<c(CN-) | |
| B. | 点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH) | |
| C. | 点③和点④所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| D. | 点②和点③所示溶液中都有:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
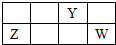 短周期元素X、Y、Z、W的原子序数依次增大,X、Y原子最外层电子数之和等于W原子最外层电子数,Y、Z的最高正化合价之和为8.部分元素在周期表中的相对位置如右图所示.下列说法中正确的是( )
短周期元素X、Y、Z、W的原子序数依次增大,X、Y原子最外层电子数之和等于W原子最外层电子数,Y、Z的最高正化合价之和为8.部分元素在周期表中的相对位置如右图所示.下列说法中正确的是( )| A. | ZY晶体熔化、ZCl3溶于水破坏的化学键种类相同 | |
| B. | 化合物YCl3水解产物之一具有强氧化性,由此可知Y在该化合物中的化合价为+3 | |
| C. | 元素R与W同主族,且原子序数小于W.因为R的非金属性强于W,所以X2R的沸点高于X2W | |
| D. | Z2W3固体可由溶液中复分解反应制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2、SO2、NH3都是直线形分子 | |
| B. | CO2、NH3、H2S 的键角依次减小 | |
| C. | H2O2、N2H4分子的中心原子都是 sp3杂化 | |
| D. | C、N、F元素的电负性依次增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
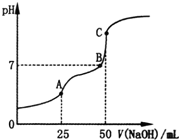
| A. | HC2O4-的电离程度大于其水解程度 | |
| B. | B点时溶液中含有Na2HC2O4和Na2C2O4 | |
| C. | C点时,c(Na+)>c(C2O42-)>c(HC2O4- )>c(OH-)>c(H+) | |
| D. | A点时,c(Na+)+c(H+)═c(OH-)+c(HC2O4-)+2c(C2O42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阳极反应为:Fe-2e-═Fe2+ | B. | 电解过程中pH不变 | ||
| C. | 过程中有Fe(OH)3生成 | D. | 上述反应中Cr2O72-被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 工业上用电解MgCl2溶液的方法冶炼Mg | |
| B. | 钢铁发生吸氧腐蚀的正极反应式为4OH--4e-═O2↑+2H2O | |
| C. | 如图中发生反应的方程式为:Fe+2H+=Fe2++H2↑ | |
| D. | 碱性锌锰干电池放电时的正极反应为:MnO2+H2O+e-=MnOOH+OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com