
【题目】下列化学用语表示正确的是![]()
![]()
A.CCl4的电子式:![]()
B.用电子式表示硫化钠的形成过程:![]()
C.14C的原子结构示意图:![]()
D.碳酸氢钙与少量氢氧化钠溶液反应:Ca2+ + 2HCO3- + 2OH- = CaCO3↓+ CO32- + 2H2O
科目:高中化学 来源: 题型:
【题目】古代有火烧孔雀石炼铜(加入炭)和湿法炼铜(在溶液中加铁),下列有关说法不正确的是( )
A. 火烧孔雀石炼铜发生的反应有Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O
B. 火烧孔雀石炼铜发生的反应有2CuO+C![]() CO2↑+2Cu
CO2↑+2Cu
C. 湿法炼铜发生的主要反应为Fe+Cu2+===Cu+Fe2+
D. 两种炼铜的方法涉及的主要反应都是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
福酚美克是一种影响机体免疫力功能的药物,可通过以下方法合成:
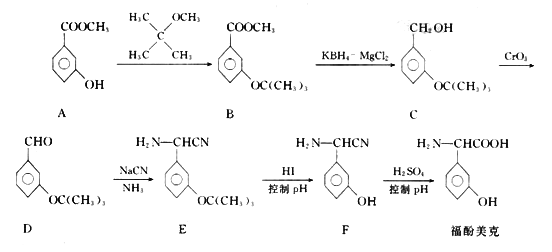
回答下列问题:
(1)物质A的含氧官能团的名称为___________;B→C的转化属于___________反应(填反应类型)
(2)上述流程中设计A→B步骤的目的是________;F分子中共平面的原子最多有________个。
(3)D与银氨溶液发生反应的化学方程式为___________。
(4)福酚美克具有多种同分异构体.写出其中符合下列条件的有机物结构简式:___________和___________。
①含有-CONH2;
②能与FeCl3溶液发生显色反应;
③核磁共振氢谱的吸收峰数目有4个。
(5)参照上述合成路线和信息,以乙醇为原料(无机试剂任选),设计制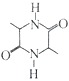 的合成路线:___________。
的合成路线:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的类别和核心元素的化合价是研究物质性质的两个重要维度。下图为硫及其部分化合物的“价类二维图”,根据图示回答下列问题:
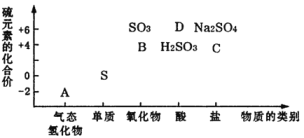
(1)根据“价类二维图”,下列能与B反应的物质有_____,反应中使B表现还原性的物质是__(填序号)。
①NaOH溶液 ②CaCl2溶液 ③酸性KMnO4溶液 ④H2S溶液
(2)C的钠盐放置在空气中极易变质,请设计实验方案证明其已被氧化___。
(3)请写出金属铜与D的浓溶液在一定条件下发生反应的化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭容器中通入lmolX和2molY,发生下列反应:X(g)+2Y(g)![]() M(g)+2N(g) △H=akJ/mol(a>0),下列说法中正确的是
M(g)+2N(g) △H=akJ/mol(a>0),下列说法中正确的是
A. 到达平衡状态时,加入催化剂,平衡不移动,反应速率也不会发生改变
B. 反应达到平衡时,X和Y的转化率相等
C. v正(X)=2v逆(N)时,反应到达平衡状态
D. 到达平衡状态时,反应吸收akJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应能通过原电池的形式来实现的是
A.Cu+2Ag+=2Ag+Cu2+B.Cu+2H+=H2↑+Cu2+
C.CaCO3+2HCl=CaCl2+CO2↑十H2OD.2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列五种有机物:①CH4、②CH2=CH2、③CH3CH2OH、④ CH3 CH2CH2 CH3 、⑤CH3COOH
请回答:
(1)写出⑤的官能团的名称______。
(2)与①互为同系物的是______(填序号)。
(3)写出④ 的同分异构体的结构简式________________。
(4)写出与②发生加成反应生成乙烷的化学方程式_________________________。
(5)③与⑤发生反应的化学方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从某矿渣(成分为NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等)中回收NiSO4的工艺流程如图:
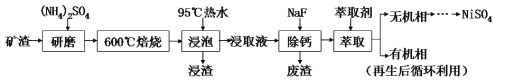
已知:(NH4)2SO4在350℃分解生成NH3和H2SO4;NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3。
回答下列问题:
(1)“研磨”的目的是___。
(2)矿渣中部分FeO在空气焙烧时与H2SO4反应生成Fe2(SO4)3的化学方程式为____。
(3)“浸泡”过程中Fe2(SO4)3生成FeO(OH)的离子方程式为___。“浸渣”的成分除Fe2O3、FeO(OH)、CaSO4外还含有___(填化学式)。
(4)向“浸取液”中加入NaF以除去溶液中Ca2+,溶液中c(F-)至少为___mol·L-1时,可使钙离子沉淀完全。[已知Ca2+浓度小于1.0×10-5mol·L-1时沉淀完全;Ksp(CaF2)=4.0×10-11]
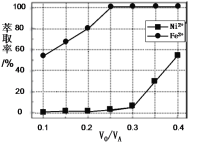
(5)萃取可用于对溶液中的金属离子进行富集与分离:Fe2+(水相)+2RH(有机相)![]() FeR2(有机相)+2H+(水相)。萃取剂与溶液的体积比(
FeR2(有机相)+2H+(水相)。萃取剂与溶液的体积比(![]() )对溶液中Ni2+、Fe2+的萃取率影响如图所示,
)对溶液中Ni2+、Fe2+的萃取率影响如图所示,![]() 的最佳值为___。在___(填“强碱性”“强酸性”或“中性”)介质中“反萃取”能使有机相再生而循环利用。
的最佳值为___。在___(填“强碱性”“强酸性”或“中性”)介质中“反萃取”能使有机相再生而循环利用。
(6)若将流程图中浸泡步骤改为如图步骤(前后步骤不变)。依据下表数据判断,调pH范围为___。
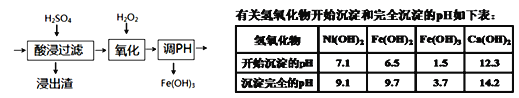
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M 均为中学化学中常见物质,一定条件下它们之间有如下转化关系(其它产物已略去)。下列说法中不正确的是( )
![]()
A.若 M 是单质铁,则 Z 溶液可能是 FeCl2 溶液
B.若 M 是氢氧化钠,则 X 水溶液呈酸性
C.若 M 是氧气,则 X、Z 的相对分子质量可能相差 48
D.若 M 是强氧化性的单质,则 X 可能是金属铝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com