
【题目】向100mL Fe2(SO4)3和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中固体剩余物的质量与加入铁粉的质量如图所示。忽略溶液体积的变化,下列说法正确的是
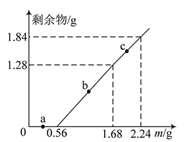
A. a点时溶液中阳离子仅为Cu2+和Fe2+
B. b点时溶液中发生的反应为:Fe+Cu2+=Cu+Fe2+
C. c点时溶液中溶质的物质的量浓度为0.5 mol·L-1
D. 原溶液中Fe2(SO4)3和CuSO4的物质的量浓度之比为1∶1
【答案】BC
【解析】A项,向100mLFe2(SO4)3和CuSO4的混合溶液中逐渐加入铁粉,先发生反应:Fe+2Fe3+=3Fe2+,后发生反应:Fe+Cu2+=Cu+Fe2+,如图加入0.56g(即0.01mol)Fe之后开始出现固体,则a点溶液中阳离子为Cu2+、Fe2+和Fe3+,故A错误;B项,由图可得,加入铁粉从0.56g~1.68g(即0.02mol)时,剩余物为1.28g,而1.28gCu的物质的量为0.02mol,所以此时发生反应为:Fe+Cu2+=Cu+Fe2+,b点在该范围内,故B正确;C项,加入铁粉为从0.56g~2.24g(即0.03mol)时,若发生反应Fe+Cu2+=Cu+Fe2+,则生成0.03mol(即1.92g)Cu,而由图示可得剩余物为1.84g,所以此时溶液中早已没有Cu2+,设0.03mol铁粉中与Cu2+反应的为x mol,剩余y mol,则生成Cu的质量为64x g,剩余铁的质量为56y g,所以x+y=0.03、64x+56y=1.84,解得:x=0.02(mol)、y=0.01(mol),因此加入铁粉从0.56g~1.68g(即0.02mol)时,刚好与溶液中的Cu2+反应完全,溶液中溶质为FeSO4,又根据前面的分析可得反应Fe+2Fe3+=3Fe2+生成Fe2+0.03mol,又因为反应Fe+Cu2+=Cu+Fe2+生成Fe2+0.02mol,所以c点时溶液中溶质的物质的量浓度为:(0.03mol+0.02mol)÷0.1L=0.5 mol·L-1,故C正确;D项,由前面的分析可得,原溶液中Fe3+为0.02mol,则Fe2(SO4)3为0.01mol,Cu2+为0.02mol,则CuSO4为0.02mol,所以原溶液中Fe2(SO4)3和CuSO4的物质的量浓度之比=物质的量之比,为1:2,故D错误。


科目:高中化学 来源: 题型:
【题目】实验室里有4个药品橱,已经存放以下物品:
药品橱 | 甲橱 | 乙橱 | 丙橱 | 丁橱 |
药品 | 盐酸,硫酸 | 氢氧化钠,氢氧化钙 | 红磷,硫 | 铜,锌 |
实验室新购进一些碘,应该将这些碘放在( )
A.甲橱B.乙橱C.丙橱D.丁橱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对乙烯基苯甲酸是重要的医药中间体,广泛应用于合成感光材料。对乙烯基苯甲酸可通过如下反应合成。
反应①: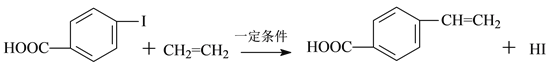
I II
(1)下列关于化合物I和化合物II的说法,正确的是______。
A.化合物I能与新制的Cu(OH)2反应
B.均可发生酯化反应和银镜反应
C.化合物II能使KMnO4溶液褪色
D.1mol化合物II最多能与5 mol H2反应
(2)化合物II的分子式为____________,化合物II在催化剂条件下生产高分子化合物的反应方程式___________________________________________________________。
(3)化合物II可由芳香族化合物Ⅲ通过消去反应获得,Ⅲ和Cu共热的产物能发生银镜反应,写出化合物Ⅲ的结构简式_______________________;
(4)化合物IV是化合物II的同分异构体,且化合物IV遇FeCl3溶液显紫色,苯环上的一氯代物只有2种,写出化合物IV的结构简式____________________________(写一种)。
(5)利用类似反应①的方法,仅以溴苯(![]() )和乳酸(
)和乳酸(![]() )为有机物原料合成化工原料肉桂酸(
)为有机物原料合成化工原料肉桂酸(![]() ),涉及的反应方程式为________________________________;___________________________________。
),涉及的反应方程式为________________________________;___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关Na2CO3和NaHCO3的性质说法正确的是
A. 溶解度:Na2CO3>NaHCO3
B. 右图所示装置可证明稳定性:Na2CO3>NaHCO3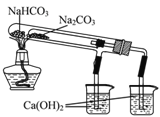
C. 用澄清石灰水可鉴别Na2CO3溶液和NaHCO3溶液
D. 等质量的Na2CO3和NaHCO3分别与过量盐酸反应,放CO2质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示(部分物质和条件已略去)。A、B、E、G、H、J常温下为气体,A为黄绿色,J为红棕色,B能使湿润的红色石蕊试纸变蓝,E是空气中含量最多的气体,C工业上用于制取漂白粉,K为一种红色金属单质,I是常见的无色液体。

(1)E的电子式为___________________。
(2)反应②的化学方程式为___________________。
(3)写出反应③的化学方程式,并用单线桥表示电子转移的方向和数目:___________________。
(4)反应⑤的离子方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“84”消毒液是一种以NaClO为主的消毒剂,广泛应用于医院、食品加工、家庭等的卫生消毒。
(1)“84”消毒液中通入CO2能增强消毒效果,写出向“84”消毒液中通入过量CO2的离子方程式:___________________。
(2)测定“84”消毒液中NaClO的物质的量浓度的方法如下:
①配制100.00mL 0.5000 mol·L-1的Na2S2O3溶液。配制过程中需准确称取Na2S2O3固体___________________g,需要用到的玻璃仪器有烧杯、胶头滴管、量筒、___________________。
②准确量取10.00 mL消毒液于锥形瓶中,加入过量的KI溶液,用足量的乙酸酸化,充分反应后向溶液中滴加Na2S2O3溶液,完全反应时消耗Na2S2O3溶液25.00 mL。反应过程中的相关离子方程式为:
2CH3COOH+2I—+ClO—=I2+Cl—+2CH3COO—+H2O,I2+2S2O![]() =2I—+S4O
=2I—+S4O![]()
通过计算求出该“84”消毒液中NaClO的物质的量浓度。(写出计算过程)__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对有机物:  的下列说法中不正确的是( )
的下列说法中不正确的是( )
A.常温下能与NaHCO3溶液反应放出CO2
B.在碱性条件下能发生水解反应,1摩该有机物完全反应消耗掉8摩NaOH
C.与稀H2SO4共热,生成2种有机物
D.该有机物的分子式为C14H10O9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质均为常见物质或它们的溶液,其中A为淡黄色固体,C、X均为无色气体,Z为浅绿色溶液,D为一种常见的强碱。根据它们之间的转化关系(下图), 用化学用语回答问题。(部分产物已省略)
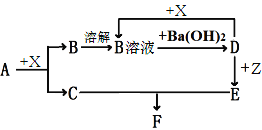
(1)写出下列物质的化学式:A______,B_______D_______。
(2)A与SO3(g)的反应类似于A与X的反应,请写出A与S03(g)反应的化学方程式_______。
(3)向Z溶液中通入一定量的Cl2,写出检验Z中阳离子是否反应充全所需试剂:______。
(4)物质E转化为物质F的现象为_____, 化学方程式为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com