
����Ŀ���������ʾ�Ϊ�������ʻ����ǵ���Һ������AΪ����ɫ���壬C��X��Ϊ��ɫ���壬ZΪdz��ɫ��Һ��DΪһ�ֳ�����ǿ���������֮���ת����ϵ����ͼ��, �û�ѧ����ش����⡣�����ֲ�����ʡ�ԣ�
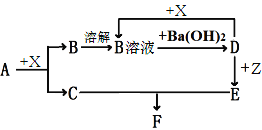
��1��д���������ʵĻ�ѧʽ��A______��B_______D_______��
��2��A��SO3(g)�ķ�Ӧ������A��X�ķ�Ӧ����д��A��S03(g)��Ӧ�Ļ�ѧ����ʽ_______��
��3����Z��Һ��ͨ��һ������Cl2��д������Z���������Ƿ�Ӧ��ȫ�����Լ���______��
��4������Eת��Ϊ����F������Ϊ_____, ��ѧ����ʽΪ______��
���𰸡� Na2O2 Na2CO3 NaOH 2SO3+2Na2O2==2Na2SO4+O2 K3Fe(CN)6����KMnO4��Һ�� ��ɫ����ת��Ϊ����ɫ����������ת��Ϊ���ɫ���� 4Fe(OH)2+2H2O+O2=4Fe(OH)3
�����������������֪��AΪ����ɫ���壬�ǹ������ƣ�ZΪdz��ɫ��Һ����������������Һ��DΪһ�ֳ�����ǿ����������ƣ��ܹ���������Ʒ�Ӧ������ɫ�������ɫ�����Ƕ�����̼�����ɵ���ɫ����Ϊ������̼����������������Һ��Ӧ�����������ƣ�
��1��ͨ�����Ϸ�����֪��A��Na2O2��B��Na2CO3�� D��NaOH����ȷ�𰸣�Na2O2��Na2CO3�� NaOH��
��2�����������������̼��Ӧ����̼���ƺ�����������������SO3(g)�ķ�Ӧ���������ƺ���������ѧ����ʽΪ��2SO3+2Na2O2==2Na2SO4+O2 ����ȷ����2SO3+2Na2O2==2Na2SO4+O2��
��3��Z��Һ�к����������ӣ�ͨ�����������������ӣ�Ҫ����Z��Һ�����������Ƿ���ڣ�������K3Fe(CN)6����KMnO4��Һ������û����ɫ�������ɻ���Һ��ɫ����˵�����������Ѿ���ȫ�������������ӣ���ȷ�𰸣�K3Fe(CN)6����KMnO4��Һ����
��4��OH- ��Fe2+��Ӧ����Fe(OH)2��ɫ���������������Ĵ����£���ɫ����������Ϊ����ɫ�����ձ�Ϊ���ɫFe(OH)3����ѧ����ʽ��4Fe(OH)2+2H2O+O2=4Fe(OH)3����ȷ�𰸣�4Fe(OH)2+2H2O+O2=4Fe(OH)3��


 ��������ϵ�д�
��������ϵ�д� ��ӡ�Ļ���ʱ����ϵ�д�
��ӡ�Ļ���ʱ����ϵ�д� ��ѧ�����ϵ�д�
��ѧ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100mL Fe2(SO4)3��CuSO4�Ļ����Һ���������ۣ���ַ�Ӧ����Һ�й���ʣ�����������������۵�������ͼ��ʾ��������Һ����ı仯������˵����ȷ����
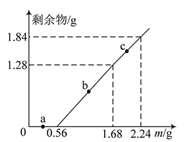
A. a��ʱ��Һ�������ӽ�ΪCu2+��Fe2+
B. b��ʱ��Һ�з����ķ�ӦΪ��Fe��Cu2+=Cu��Fe2+
C. c��ʱ��Һ�����ʵ����ʵ���Ũ��Ϊ0.5 mol��L��1
D. ԭ��Һ��Fe2(SO4)3��CuSO4�����ʵ���Ũ��֮��Ϊ1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л����˵����ȷ���ǣ� ��
A.���ࡢ��֬�������ʶ��Ǹ߷��ӻ�����
B.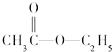 �� H
�� H ![]() O����ˮ�ⷴӦ�����ɵIJ�����18O�������Ҵ���
O����ˮ�ⷴӦ�����ɵIJ�����18O�������Ҵ���
C.��ȥ���������л��е����ᣬ���Լ����Ҵ���������
D.��֬����������������ˮ�ⶼ���ɱ����������ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ҩƷ�DZ�ˮ�����ϳ�·����ͼ���ش��������⣺ 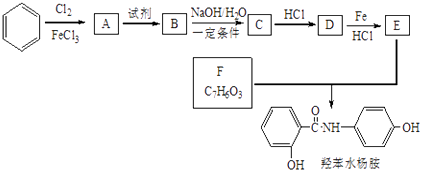
��֪�� 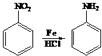
��1���DZ�ˮ��ķ���ʽΪ �� �����DZ�ˮ�������˵����ȷ���ǣ�����ţ���
a.1mol�DZ�ˮ������Ժ�2mol NaOH��Ӧ
b�����ܷ���������Ӧ
c���ɷ���ˮ�ⷴӦ
d�������巢��ȡ����Ӧ
��2��D������Ϊ ��
��3��A��B�����Լ�Ϊ��D��E��Ӧ���л���Ӧ������ ��
��4��B��C��Ӧ�Ļ�ѧ����ʽΪ ��
��5��д�� F��ͬ���칹���м�����FeCl3������ɫ��Ӧ�����ܷ���������Ӧ�ģ������к˴Ź���������ʾ4��壬�ҷ����֮��Ϊ1��2��2��1��ͬ���칹���һ�ֽṹ��ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.ij�������糧��úΪȼ�ϣ��ų��ķ����к���CO2��SO2��ˮ������Ϊ����÷����еijɷ֣�����ͼ��ʾ��װ�ý���ʵ�飺

��1���������ӵ�˳��Ϊ(��ܽӿ���ĸ) ��
��2������ ����֤����CO2��
��3��װ��B�������� ��װ��D�������� ��
II. Ϊ̽��SO2��Ư����SO2ֱ����������ɫ���ʣ�����SO2��ˮ��Ӧ�IJ�������ã������ͼװ�ý���ʵ�飺��ͼ�������������������Ϊ70����

��4������������Ũ���ᷴӦ�Ļ�ѧ����ʽ�� ��
��5��Ϊ̽�������SO2 �ܲ���ʹƷ����ɫ����ָ����Ƶ�ʵ��װ��ͼ���������ԵIJ��㣺
�� ��
�� ��
��6�������ĺ��װ�ã�ʵ���п���SO2�Դ�Լÿ��3�����ݵ��ٶ�ͨ��Ʒ��ľƾ���Һʱ������һСʱ��Ʒ���Բ���ɫ����˵��Ʒ����ɫ��ԭ����SO2ֱ�ӵ��¡����ԣ�SO2 ͨ��Ʒ��ˮ��Һ������Ʒ����ɫ���������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������и�װ��ͼ������������ȷ����

A. ������װ�â�������������c��Ϊ������d��Ϊ�������������ҺΪAgNO3��Һ
B. װ�â���ԭ��أ��ܽ���ѧ��ת��Ϊ���ܣ�SO42������п�缫
C. װ�â���X��Ϊ���Ȼ�̼���������հ������Ȼ��⣬��������
D. װ�âܿ������ռ������������ն���İ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����ڱ���ǰ�����ڵ�����Ԫ��A��B��C��D��E��F�˵����������������Aԭ�Ӻ���������δ�ɶԵ��ӣ�������B2E�ľ���Ϊ���Ӿ��壬Eԭ�Ӻ����M���������ԳɶԵ��ӣ�CԪ���ǵ��к�����ߵĽ���Ԫ�أ�D���ʵ��۵���ͬ����Ԫ���γɵĵ���������ߵģ�F2�����Ӻ��������Ӿ������������������Ϣ���ش��������⣺
��1��A��B��C��D�ĵ�һ��������С�����˳��Ϊ______����Ԫ�ط��ű�ʾ��
��2��B���Ȼ�����۵��D���Ȼ�����۵�ߣ�������______��
��3��E�������������ӵĿռ乹����______����______���ӣ�����ԡ����Ǽ��ԡ���
��4��Fԭ�ӵļ۲�����Ų�ʽ��_____��
��5��E��F�γ�ij�ֻ���������ͼ��ʾ���־���ṹ����ɫ���ʾFԭ�ӣ����仯ѧʽΪ_____����a����Eԭ�ӵ���λ��Ϊ______�����ڣ�b���Ľṹ��ȡ��һ��ƽ����������Ϊ��������ƽ��һ�������к���_____��Fԭ�ӡ��ṹ��a���루b���о�����ԭ�ӿռ���������ȣ���a��________��b�����>����<����=����
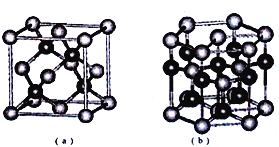
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤����������ֵ������������ȷ����
A. 78g���к��е�̼̼˫������ĿΪ3NA
B. 16gCu2S��CuO��ɵĻ�����к��е���������Ϊ0.2NA
C. ��1mol H2�� 1 mol I2����һ�ܱ������г�ַ�Ӧ��ת�Ƶĵ�����Ϊ2NA
D. 1 mol Fe ��������Ũ���Ṳ�ȷ�Ӧ������SO2�ķ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�����������ǣ� ��
A.����ʱ��Ӧʹ�¶ȼ�ˮ����������ƿ֧�ܿ�
B.��Һʱ����Һ©�����²�Һ����¿ڷų����ϲ�Һ����Ͽڵ���
C.��ȡ����Һǰ��Է�Һ©����©
D.�þƾ���ȡ��ˮ�еĵ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com