
【题目】胶体区别于其它分散系的本质是()
A. 胶体粒子不能穿过半透膜,能通过滤纸空隙
B. 胶体粒子带电荷并且在一定条件下能稳定存在
C. 胶体的分散质粒子直径在1 nm~100nm之间
D. 胶体粒子能够发生布朗运动而且能产生丁达尔现象
科目:高中化学 来源: 题型:
【题目】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
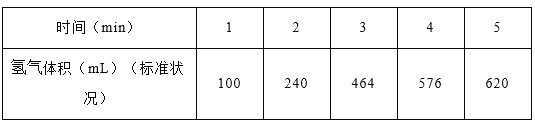
①哪一时间段反应速率最大______min(填0~1、1~2、2~3、3~4、4~5),原因是_____。
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率_________(设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是____。
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
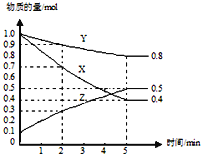
①该反应的化学方程式是_______。
②该反应达到平衡状态的标志是______
A.Y的体积分数在混合气体中保持不变
B.X、Y的反应速率比为3∶1
C.容器内气体压强保持不变
D.容器内气体的总质量保持不变
E.生成1mol Y的同时消耗2mol Z
③2min内Y的转化率为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用已知浓度盐酸滴定未知浓度的NaOH溶液,以酚酞作指示剂,下列操作会使所测NaOH溶液浓度偏低的是( )
A.锥形瓶洗净后还留有蒸馏水
B.取碱液的滴定管开始有气泡,放出液体后气泡消失
C.溶液颜色较浅时滴入酸液过快,停止滴定后反加一滴NaOH溶液无变化
D.用碱式滴定管取一定体积的NaOH溶液时,量取前仰视读数,量取后俯视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池是将化学能转变为电能的装置。关于下图所示原电池的说法不正确的是
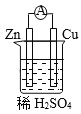
A. Cu为正极,Zn为负极 B. 电子由铜片通过导线流向锌片
C. 正极反应式为2H+ + 2e- ![]() H2↑ D. 原电池的反应本质是氧化还原反应
H2↑ D. 原电池的反应本质是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关几种常见的金属和非金属及其化合物的说法正确的是( )
A.铝热反应是指铝能将所有的金属从其氧化物中置换出来
B.Na,Mg,Al,Fe,Cu都能导电,它们的氧化物都能与酸反应
C.CO2 , NO,SO2都是非金属氧化物,都属于酸性氧化物
D.CaCO3+SiO2 ![]() ?CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸
?CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mL HNO3和H2SO4的混合溶液中,两种酸的物质的量浓度之和为0.6mol/L。向该溶液中加入足量的铜粉,加热,充分反应后,所得溶液中Cu2+的物质的量浓度最大值为(反应前后溶液体积变化忽略不计)
A. 0.225mol/L B. 0.30mol/L C. 0.36mol/L D. 0.45mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。
![]()
(1)若A是一种活泼金属,C是淡黄色固体,试用化学方程式表示该物质C的一个重要应用 ;
(2)若A是一种黄色单质固体,则B→C的化学方程式为 ;
(3)若A是一种黑色非金属单质固体,写出B的一个用途 ;
(4)若C是红棕色气体,则A化学式可能为 ,试写出C与水反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把7.2g铁粉投入40ml某HNO3溶液中,充分反应后剩余固体1.6g,产生NO2和NO的混合气体0.08mol,若不考虑N2O4的存在,则原HNO3溶液的物质的量浓度( )
A.3.5 mol/L
B.4.5 mol/L
C.7.0 mol/L
D.9.0 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现将浓度相等、体积分别为V1、V2的H2SO4、NaOH溶液混合,测量混合液温度,结果如图(已知:V1+V2=60mL)。下列叙述错误的是 ( )

A. 实验的环境温度低于22℃ B. 混合溶液的导电能力:M>N
C. P点混合溶液呈中性 D. 若将H2SO4改为CH3COOH,P点温度低于28℃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com