
【题目】下列变化中需加入氧化剂才能实现的是( )。
A. Cl-→Cl2 B. Fe3+→Fe2+ C. CuO→Cu D. H2SO4→BaSO4
科目:高中化学 来源: 题型:
【题目】萜品醇可作为消毒剂、抗氧化剂、医药和溶剂。合成α-萜品醇G的路线之一如下:

已知: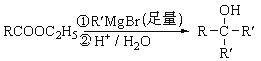
请回答下列问题:
(1)A的分子式为______;G所含官能团的名称是______。
(2)C→D的反应类型为____;该反应的副产物中与D互为同分异构体的化合物的结构简式为______。
(3)E→F反应中加入试剂浓H2SO4的作用是_______;F中混有少量C2H5OH和E,最好用_____(填字母)洗涤除去。
A.水 B.氢氧化钠溶液 C.浓硫酸 D.饱和碳酸钠溶液
(5)B在一定条件下发生聚合反应的化学方程式为______;写出同时满足下列条件的B的链状同分异构体的结构简式________。
①核磁共振氢谱有2个吸收峰。 ②能发生银镜反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】压强对合成氨反应具有重要的影响。下表是反应达到平衡时压强与NH3含量的一些实验数据:
压强/MPa | 10 | 20 | 30 | 60 | 100 |
NH3含量(体积分数)/% | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
从表中数据可以推断:随着压强增大,平衡时NH3含量
A. 增加 B. 减少 C. 先增加,后减 D. 先减少,后增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一支50mL酸式滴定管其中盛有溶液,液面恰好在10mL刻度处,现把管内溶液全部流下排出,用量筒盛装,该溶液的体积应为
A. 10mL B. 40mL C. 大于40mL D. 小于40mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒电池以惰性材料做电解,在电解质溶液中发生的总反应式为:
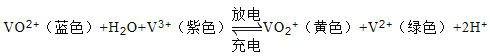
下列说法正确的是( )
A.当电池放电时,VO2+离子被氧化
B.放电时,负极反应为:VO2+ +2H+ +2e- =VO2+ +H2O
C.充电时,阳极附近溶液由绿色逐渐变为紫色
D.放电过程中,正极附近溶液的pH变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用氧化铝基废催化剂(主要成分为Al2O3,少量Pd)回收Al2(SO4)3及Pd的流程如下:
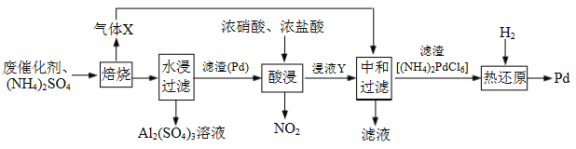
⑴焙烧时产生的气体X为_____________(填化学式)。
⑵浸液Y的主要成分为_____________(填化学式)。
⑶“热还原”过程中发生反应的化学方程式为____________。
⑷上述流程中焙烧温度不宜过高,否则会导致硫酸铵固体的分解。某兴趣小组为探究高温下硫酸铵的分解产物,通过下列装置进行实验,观察到B中溶液颜色变浅,C中无明显现象。
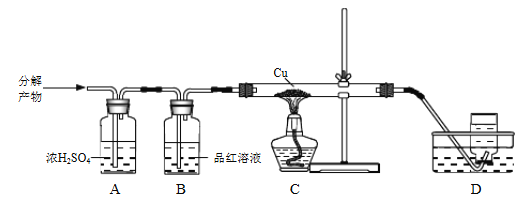
①装置B的作用是_____________。
②进一步测定可知,D中收集到的气体相对分子质量为28。写出(NH4)2SO4固体高温分解的化学方程式:_____________。
⑸Pd是优良的储氢金属,其储氢原理为2Pd(s)+x H2(g)=2PdHx(s),其中x的最大值为0.8。已知:Pd的密度为12g·cm-3,则1cm3Pd能够储存标准状况下H2的最大体积为
_____________L(计算结果保留整数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是合成氨的重要原料,合成氨反应的热化方程式如下:
N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ/mol
2NH3(g) ΔH=-92.4 kJ/mol
(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如下图所示。
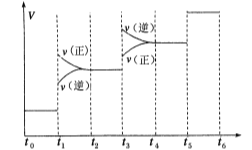
图中t1时引起平衡移动的条件可能是 ,其中表示平衡混合物中NH3的含量最高的一段时间是 ,若t0-t1,t1-t3,t3-t5这三段平衡常数分别用K1,K2,K3表示,那么K1,K2,K3的大小关系是____________。
(2)若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”、“ 向右”或“不”);使用催化剂反应的ΔH (填“增大”、“减小”或“不改变”)。
(3)温度为T ℃时,将2a mol H2和 a mol N2放入0.5 L密闭容器中,充分反应后测得N2的转化率为50%。则反应的平衡常数为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com