
【题目】(2017·浙江省温州中学高三3月模拟)以下是对某水溶液进行离子检验的方法和结论,其中正确的是
A.先加入BaCl2溶液,再加入足量的HNO3溶液,产生了白色沉淀。溶液中一定含有大量的![]()
B.加入足量的CaCl2溶液,产生了白色沉淀。溶液中一定含有大量的![]()
C.加入足量浓 NaOH溶液,产生了带有强烈刺激性气味的气体,该气体可以使湿润的红色石蕊试纸变蓝,则溶液中一定含有大量的![]()
D.先加适量的盐酸将溶液酸化,再加AgNO3溶液,产生了白色沉淀。溶液中一定含有大量的Cl
 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:
【题目】14C常用于测定生物遗骸的年份。下列说法正确的是
A. 14C含有14个中子 B. 14C与14N含有相同的质子数
C. 14C与C60互为同位素 D. 14C与12C是两种不同的核素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中A到F是化合物,且A、B、E、F均含钠元素,G是单质.

(1)写出A、B、E、F的化学式:A________,B________,E________,F________.
(2)写出反应①②③的化学方程式:① _____________________________② _________________________________③__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸是重要的化工原料,在生活、生产中被广泛应用。
(1)写出乙酸在水溶液中的电离方程式_______________________。若某温度下,CH3COOH(aq)与NaOH(aq)反应的焓变△H= - 46.8kJ·mol-1 ,HCl(aq)与NaOH(aq)反应的焓变△H= - 55.6 kJ·mol-1,则CH3COOH在水中电离的焓变△H=_________kJ·mol-1。
(2)已知常温下CH3COOH的电离常数K=1.6×10-5,该温度下,1 mol·L-1CH3COONa溶液pH约为________(已知lg2=0.3)。向pH=2的CH3COOH溶液中加入pH=2的稀硫酸溶液,保持溶液温度不变,溶液的pH将________________填“变大”或“变小”或“不变”)。
(3)常温下,向10 mL 0.1 mol·L-1的CH3COOH溶液中逐滴滴入0.1 mol·L-1的ROH溶液,所得溶液pH及导电性变化如图。下列分析正确的是_______。

A.b点导电能力最强,说明ROH为强碱
B.b点溶液pH=5,此时酸碱恰好中和
C.c点溶液存在c(R+)>c(CH3COO-)、c(OH-)>c(H+)
D.b~c任意点溶液均有c(H+)·c(OH-)=KW=1.0×10-14
(4)近年来用乙烯和乙酸为原料、杂多酸作催化剂合成乙酸乙酯的新工艺,具有明显经济优势。其合成的基本反应如下:![]()
①在恒温恒容容器中投入一定量的乙烯和足量的乙酸,下列分析正确的是________。
A.当乙烯断开1mol碳碳双键的同时乙酸恰好消耗1mol,说明反应已达到化学平衡
B.当体系中乙烯的百分含量保持不变,说明反应已达到化学平衡
C.达到化学平衡后再通入少量乙烯,再次达到化学平衡时,乙烯的浓度与原平衡相等
D.该反应的平衡常数表达式为K=![]()
②乙烯与乙酸等物质的量投料条件下,某研究小组在不同压强下进行了在相同时间点乙酸乙酯的产率随温度的变化的测定实验,实验结果如图所示。回答下列问题:
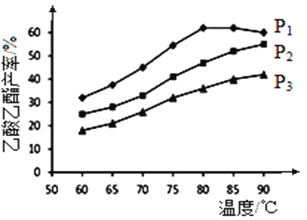
温度在60~80℃范围内,乙烯与乙酸反应速率由大到小的顺序是__________________[用![]() (P1)、
(P1)、![]() (P2)、
(P2)、![]() (P3)分别表示不同压强下的反应速率]。在压强为P1MPa、温度超过80℃时,乙酸乙酯产率下降的原因可能是___________________________。根据测定实验结果分析,较适宜的生产条件是_________________(填出合适的压强和温度)。为提高乙酸乙酯的合成速率和产率,可以采取的措施有___________________(任写出一条)。
(P3)分别表示不同压强下的反应速率]。在压强为P1MPa、温度超过80℃时,乙酸乙酯产率下降的原因可能是___________________________。根据测定实验结果分析,较适宜的生产条件是_________________(填出合适的压强和温度)。为提高乙酸乙酯的合成速率和产率,可以采取的措施有___________________(任写出一条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温、同压下,在3支体积相同的试管中分别充有体积比为1:1的两种气体组成的混合气体,它们是:①NO、NO2;②NO2、O2;③NH3、N2。现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积大小关系正确的是
A. ①>②>③ B. ①=③>② C. ②>③>① D. ③>①>②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于碰撞的说法正确的是( )
A. 活化分子之间的碰撞一定能引发化学反应,即活化分子之间的碰撞为有效碰撞
B. 发生有效碰撞的分子必为活化分子
C. 反应物分子之间的碰撞一定会引发化学键的断裂
D. 反应物分子之间只要有合适的取向的碰撞必为有效碰撞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)阅读、分析下列两个材料:
材料一
物质 | 熔点/℃ | 沸点/℃ | 密度/g/cm3 | 溶解性 |
乙二醇 | 11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
材料二

回答下列问题(填序号):
A.蒸馏法 B.萃取法 C.“溶解、结晶、过滤”的方法 D.分液法
①将纯碱从氯化钠和纯碱的混合物中分离出来,最好用 ;
②将乙二醇和丙三醇相互分离的最佳方法是___________。
(2)阅读材料三
在溶解性方面,Br2(溴)与I2很相似,其稀的水溶液显黄色。在实验室里从溴水(Br2的水溶液)中提取Br2和提取I2的方法相似。
回答下列问题:
①常用的提取方法是____________,化学试剂是 ,最主要的仪器是 。
②若观察发现提取Br2以后的水还有颜色,解决该问题的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 乙酸和甲酸甲酯互为同分异构体
B. 乙烯可以用作生产食品包装材料的原料
C. 鸡蛋消溶液中加入稀(NH4)2SO4溶液后产生沉淀,是因为蛋白质发生了盐析
D. a-氨基丙酸与a-氨基苯丙酸混合物脱水成肽,只生成2种二肽
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应中,SO2做氧化剂的是( )
A. SO2+2H2S═3S+2H2O B. SO2+2NaOH═Na2SO3+H2O
C. 2SO2+O2═2SO3 D. SO2+H2O═H2SO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com