
【题目】回答下列问题:
利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,所设计的装置如下图所示:
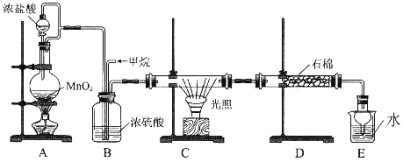
(1)最简单烷烃的空间结构为_______________。
(2)写出装置C中生成一氯甲烷的化学方程式:__________,该反应类型为:_________。
(3)D中石棉上吸附着潮湿的KI粉末,其作用是_________________________。
(4)若题目中甲烷与氯气的体积之比为1∶1,两者反应则得到的产物有____种,其中常温下为气态的有机产物的化学式为:________。
(5)将0.4molCH4与Cl2发生取代,测得4种有机取代物的物质的量相等,则消耗的氯气的物质的量是______________。
(6)烃A为甲烷的同系物,A中有12个氢原子,写出A的同分异构体中,含4个-CH3的结构简式: _________。
【答案】正四面体 CH4+Cl2![]() CH3Cl+HCl 取代反应 吸收过量的氯气 5 CH3Cl 1mol
CH3Cl+HCl 取代反应 吸收过量的氯气 5 CH3Cl 1mol 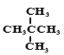
【解析】
该装置利用MnO2和浓盐酸反应制取的Cl2和甲烷光照条件下反应生成氯甲烷,并回收氯化氢气体,A装置利用MnO2和浓盐酸反应制取的Cl2,B装置将A装置中生成的Cl2同甲烷混合流入C装置,C装置在光照的条件下使甲烷和氯气发生反应,D装置中的石棉可以吸收未参加反应的Cl2,E装置用于吸收反应生成的氯化氢,据此分析。
(1)最简单的烷烃为甲烷,其空间构型为正四面体形;
(2)C装置为甲烷和氯气的反应装置,装置中反应过程复杂,甲烷和氯气反应生成一氯甲烷的反应方程式为CH4+Cl2![]() CH3Cl+HCl,属于取代反应;
CH3Cl+HCl,属于取代反应;
(3)D装置的石棉中含有KI,可以与没参加反应的Cl2反应,用于吸收未参加反应的Cl2;
(4)有机反应较为复杂,甲烷与氯气的取代反应产物中含有四种氯代甲烷和氯化氢,共5种;其中为气态的有机产物为CH3Cl;
(5)0.4mol甲烷含0.4molC原子,所以四种有机取代物各0.1mol,含Cl=0.1×(1+2+3+4)=1mol,所以消耗氯气为1mol,生成1molHCl;
(6)烃A为甲烷的同系物,则烃A为烷烃,该烷烃含有12个H原子,根据烷烃通式,烷烃A的化学式为C5H12,其同分异构体有3种,其中含有4个甲基的同分异构体为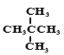 。
。


科目:高中化学 来源: 题型:
【题目】某同学设计实验以探究元素性质的递变规律,实验装置如图所示.

实验Ⅰ:根据元素最高价含氧酸的酸性强弱探究元素非金属性递变规律.
已知A装置的烧瓶里装有大理石,分液漏斗里装有稀HNO3,B装置中装有饱和碳酸氢钠溶液,装置C中装有Na2SiO3溶液,试回答:
(1)A中反应的离子方程式为 ,C中可观察到的现象是 .
(2)B装置的作用是 .
(3)根据实验现象推知,碳酸、硝酸、硅酸的酸性强弱顺序是 ,由此得出碳、硅、氮三种元素非金属性的强弱顺序是 .
实验Ⅱ:已知常温下高锰酸钾与浓盐酸混合可产生氯气,利用该装置探究氯和溴元素的非金属性强弱.
(4)写出B装置中发生反应的离子方程式: .
(5)C装置的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究氮、氯等单质及其化合物的反应有重要意义。
(1)科学家研究在一定条件下通过下列反应制备NH3:
![]()
①在其他条件相同时,反应中NH3的体积分数(a)在不同温度下随反应时间(t)的变化如图。该反应的平衡常数表达式K=______,该反应中的![]() ____0(填“>”“<”或“=”)。
____0(填“>”“<”或“=”)。
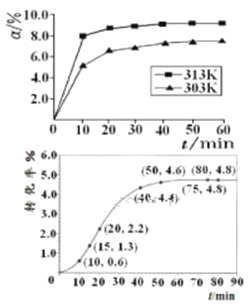
②某温度下,在2L容积不变的密闭容器中加入1molN2和6molH2O(1)发生反应,N2转化率随时间(t)变化如图。15-20min内,v(NH3)=____。若其他条件不变,在图中画出使用催化剂后N2的转化率随反应时间变化的曲线示意图_______。
(2) 25℃时,某同学将0.lmol![]() 盐酸与0.2 mol
盐酸与0.2 mol![]() 氨水等体积混合,所得混合溶液pH______7(填“>”“<”或“=”,下同),混合溶液中c(NH4+)______c(NH3
氨水等体积混合,所得混合溶液pH______7(填“>”“<”或“=”,下同),混合溶液中c(NH4+)______c(NH3![]() H2O)(25℃时,NH3.H2O的电离常数
H2O)(25℃时,NH3.H2O的电离常数![]() )
)
(3) 25℃时,向0.lmol![]() 的MgCl2溶液中逐滴加入适量0.lmol
的MgCl2溶液中逐滴加入适量0.lmol![]() 氨水,有白色沉淀生成,向反应后的浊液中,继续加入0.lmol
氨水,有白色沉淀生成,向反应后的浊液中,继续加入0.lmol![]() 的FeCl3溶液,观察到的现象是______ ;上述过程中发生的所有反应的离子方程式为______。(25℃时,
的FeCl3溶液,观察到的现象是______ ;上述过程中发生的所有反应的离子方程式为______。(25℃时,![]() ,
,![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将10 mol H2和5 mol N2放入10 L真空密闭容器内,一定温度下发生如下反应:3H2(g)+N2(g) ![]() 2NH3(g),在最初的0.2 s内,消耗H2的平均速率为0.06 mol·L1·s1,则在0.2 s末,容器中NH3的物质的量是
2NH3(g),在最初的0.2 s内,消耗H2的平均速率为0.06 mol·L1·s1,则在0.2 s末,容器中NH3的物质的量是
A. 0.12 molB. 0.08 molC. 0.04 molD. 0.8 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代社会应用最广泛的能源之一
(1)某原电池装置如图所示:

①其中,Zn电极为原电池的____ 极,电极反应式是_________________。
②Cu电极上发生的反应属于______(填“氧化”或“还原”)反应,当铜表面析出4.48 L氢气(标准状况)时,导线中通过了______ mol电子。
(2)依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示:

请回答下列问题:
①电极X的材料是______; 正极上发生的电极反应式为____________;
②当导线中通过了0.1mol电子时,银棒增重______ g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Favorskii反应是化工生产中的重要反应,它是利用炔烃与羰基化合物在强碱性下发生反应,得到炔醇,反应原理为: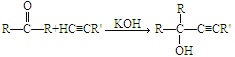
已知: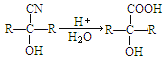
以下合成路线是某化工厂生产流程的一部分:
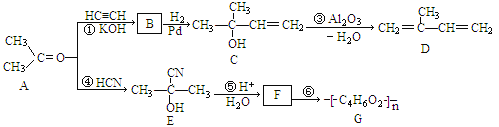
请回答下列问题:
(1)写出F中官能团的名称_________。
(2)写出D的名称(系统命名)_____________。
(3)④的反应类型是___________;B的结构简式是____________。
(4)写出反应⑥的化学方程式为_________________________________。
(5)H是D的同分异构体,核磁共振氢谱有3种峰且属于炔烃的结构简式为________________________、________________________。
(6)有关C的说法正确的是___________
A.能使溴的四氯化碳溶液褪色
B.能和氢氧化钠溶液反应
C.能使酸性高锰酸钾褪色
D.能与乙酸发生酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子中,各分子的空间构型、中心原子的杂化方式以及孤电子对数均正确的是
选项 | 分子 | 空间构型 | 杂化方式 | 孤电子对数 |
A | NH3 | 平面三角形 | sp3杂化 | N含有一对孤电子对 |
B | CCl4 | 正四面体 | sp3杂化 | C不含有孤电子对 |
C | H2O | V形 | sp2杂化 | O含有两对孤电子对 |
D | CO32- | 三角锥形 | sp3杂化 | C含有一对孤电子对 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某碱浸液中c(MoO42-)=0.80mol·L1,c(SO42-)=0.04 mol·L1,在结晶前需加入Ba(OH)2固体以除去溶液中的SO42-。当BaMoO4开始沉淀时,SO42-的去除率是( )
[Ksp(BaSO4)=1.1× 1010、Ksp(BaMoO4)=4.0 ×108,溶液体积变化可忽略不计]
A. 79.6%B. 85.6%C. 94.5%D. 98.9%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为对10 mL一定物质的量浓度的盐酸X用一定物质的量浓度的NaOH溶液Y滴定的图像,依据图像推出X和Y的物质的量浓度是下表内各组中的( )

A | B | C | D | |
X/(mol/L) | 0.12 | 0.04 | 0.03 | 0.09 |
Y/(mol/L) | 0.04 | 0.12 | 0.09 | 0.03 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com