
【题目】某同学设计实验以探究元素性质的递变规律,实验装置如图所示.

实验Ⅰ:根据元素最高价含氧酸的酸性强弱探究元素非金属性递变规律.
已知A装置的烧瓶里装有大理石,分液漏斗里装有稀HNO3,B装置中装有饱和碳酸氢钠溶液,装置C中装有Na2SiO3溶液,试回答:
(1)A中反应的离子方程式为 ,C中可观察到的现象是 .
(2)B装置的作用是 .
(3)根据实验现象推知,碳酸、硝酸、硅酸的酸性强弱顺序是 ,由此得出碳、硅、氮三种元素非金属性的强弱顺序是 .
实验Ⅱ:已知常温下高锰酸钾与浓盐酸混合可产生氯气,利用该装置探究氯和溴元素的非金属性强弱.
(4)写出B装置中发生反应的离子方程式: .
(5)C装置的作用是 .
【答案】实验Ⅰ:(1)CaCO3+2H+=Ca2++CO2↑+H2O;溶液变浑浊;
(2)除去二氧化碳中混有的硝酸蒸气;
(3)硝酸、碳酸、硅酸;N>C>Si.
实验Ⅱ:(4)2Br﹣+Cl2Br2+2Cl﹣;
(5)吸收尾气.
【解析】试题分析:实验Ⅰ:元素最高价含氧酸的酸性强弱判断元素非金属性强弱,酸性越强,非金属性越强,A中反应是碳酸钙和稀硝酸反应生成二氧化碳,证明氮非金属性大于碳;B装置是为了吸收挥发出的硝酸蒸气,避免证明碳的非金属性大于硅的实验,C中为Na2SiO3溶液,二氧化碳通入反应生成硅酸沉淀,证明碳的非金属性大于硅.
(1)A中反应是碳酸钙和稀硝酸反应生成二氧化碳,证明氮非金属性大于碳;C中为Na2SiO3溶液,二氧化碳通入反应生成硅酸沉淀,证明碳的非金属性大于硅;
(2)B装置是为了吸收挥发出的硝酸蒸气,避免证明碳的非金属性大于硅的实验;
(3)根据实验现象和元素最高价含氧酸的酸性强弱判断元素非金属性强弱,酸性越强,非金属性越强,推知C、N、Si三种元素非金属性的强弱;
实验Ⅱ:探究氯、溴的非金属性强弱的递变规律,根据实验装置图可知,实验原理为A装置:浓盐酸与高锰酸钾反应生成氯气,氯气通入装置B:溴化钾溶液中,溶液出现红色,有溴单质生成,说明氯的非金属性强于溴,装置中挥发出来的溴或氯气都有毒,会污染空气,所以要用装置C:氢氧化钠溶液吸收.
(4)氯气通入溴化钾溶液中,溴离子被氯气氧化成溴单质,据此书写离子方程式;
(5)吸收尾气.
解:实验Ⅰ:(1)A中反应是碳酸钙和稀硝酸反应生成二氧化碳,反应的离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O,根据强酸制取弱酸的原理,硝酸的酸性强于碳酸,硝酸、碳酸分别为N、C的最高价含氧酸,所以可证明氮非金属性大于碳,C中为Na2SiO3溶液,二氧化碳通入反应生成硅酸沉淀,根据强酸制取弱酸的原理,碳酸的酸性强于硅酸,碳酸、硅酸分别为C、Si的最高价含氧酸,所以可证明碳的非金属性大于硅,C装置中观察到溶液变浑浊,
故答案为:CaCO3+2H+=Ca2++CO2↑+H2O;溶液变浑浊;
(2)硝酸易挥发,制取的二氧化碳中含有硝酸,若不除去硝酸,无法说明C装置中观察到溶液变浑浊是硝酸和硅酸盐反应,还是碳酸和硅酸盐反应,所以B装置是为了吸收挥发出的硝酸蒸气,
故答案为:除去二氧化碳中混有的硝酸蒸气;
(3)A中反应是碳酸钙和稀硝酸反应生成二氧化碳,C中为Na2SiO3溶液,二氧化碳通入反应生成硅酸沉淀,证明碳酸的酸性强于硅酸,所以碳酸、硝酸、硅酸的酸性强弱顺序是硝酸、碳酸、硅酸,根据实验现象和元素最高价含氧酸的酸性强弱判断元素非金属性强弱,酸性越强,非金属性越强,推知C、N、Si三种元素非金属性的强弱为N>C>Si,
故答案为:硝酸、碳酸、硅酸;N>C>Si.
实验Ⅱ:(4)A装置:浓盐酸与高锰酸钾反应生成氯气2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,氯气通入装置B:溴化钾溶液中,2Br﹣+Cl2Br2+2Cl﹣溶液出现红色,有溴单质生成,说明氯的非金属性强于溴,
故答案为:2Br﹣+Cl2Br2+2Cl﹣;
(5)装置中挥发出来的溴或氯气都有毒,会污染空气,氢氧化钠能吸收溴单质、氯气,所以要用装置C:氢氧化钠溶液吸收,故答案为:吸收尾气.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】航天飞机常采用新型燃料电池作为电能来源,燃料电池一般指采用H2、CH4、CO、C2H5OH等可燃物质与O2一起构成的电池装置。它可直接将化学能转化为电能,甲烷燃料电池以KOH溶液为电解质,其总反应的化学方程式为:CH4+2O2+2OH-=![]() +3H2O。
+3H2O。
(1)负极上的电极反应为________。
(2)正极上的电极反应为________。
(3)消耗标准状况下的5.6 L O2时,有________ mol电子发生转移。
(4)开始放电时,正极附近溶液的pH________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA是阿伏加徳罗常数的值,下列说法正确的是
A.12g石墨烯(单层石墨)中含有六元环的个数为2NA
B.标准状况下,22.4LHF中含有的氟原子数目为NA
C.密闭容器中,lmolNH3和lmolHC1反应后气体分子总数为NA
D.在1L 0.1 mol/L的硫化钠溶液中,阴离子总数大于0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯佐卡因是局部麻醉药,常用于手术后创伤止痛、溃疡痛等,其结构简式如图所示,下列关于苯佐卡因的叙述正确的是( )
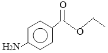
A. 分子中含有3种官能团
B. 1 mol该化合物最多与4 mol氢气发生加成反应
C. 苯环上有2个取代基,且含有硝基的同分异构体有15种
D. 分子式为C9H10NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述和方程式书写都正确的是
A.表示乙醇燃烧热的热化学方程式:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) △H= -1367.0 kJ/mol
B.KAl(SO4)2溶液中加入Ba(OH)2溶液使沉淀物质的量达到最大:Al3++2SO42-+2Ba2++4OH-= AlO2-+2BaSO4↓+2H2O
C.用稀硫酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2 =2Mn2++5O2↑+8H2O
D.用石墨作电极电解NaCl溶液:2Cl-+2H+![]() Cl2↑+H2↑
Cl2↑+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C5H7Cl的有机物,其结构不可能是( )
A. 分子中只有一个双键
B. 分子中可能有两个双键
C. 分子中可能含有一个叁键
D. 分子中可能含有一个双键和一个环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两种新型的应用于液晶和医药的材料W和Z,可用以下路线合成。
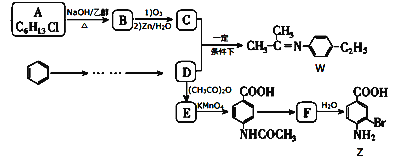
已知以下信息:
① (R1、R2、R3、R4为氢原子或烷烃基)
(R1、R2、R3、R4为氢原子或烷烃基)
②1molB经上述反应可生成2molC,且C不能发生银镜反应
③![]() (易被氧化)
(易被氧化)
④![]() +CH3-CH=CH2
+CH3-CH=CH2 ![]()
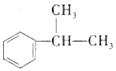
请回答下列问题:
(1)化合物A的结构简式____________,A→B的反应类型为_______________。
(2)下列有关说法正确的是____________(填字母)。
A.化合物B中所有碳原子不在同一个平面上
B.化合物W的分子式为C11H16N
C.化合物Z的合成过程中,D→E步骤为了保护氨基
D.1mol的F最多可以和4 molH2反应
(3)C+D→W的化学方程式是________________________。
(4)写出同时符合下列条件的Z的所有同分异构体的结构简式:_____________________。
①遇FeCl3溶液显紫色;
②红外光谱检测表明分子中含有![]() 结构;
结构;
③1H-NMR谱显示分子中含有苯环,且苯环上有两种不同化学环境的氢原子。
(5)设计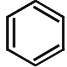 →D合成路线(用流程图表示,乙烯原料必用,其它无机过剂及溶剂任选)______________。
→D合成路线(用流程图表示,乙烯原料必用,其它无机过剂及溶剂任选)______________。
示例:CH3CHO ![]() CH3COOH
CH3COOH ![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知煤的近代结构模型如图所示。
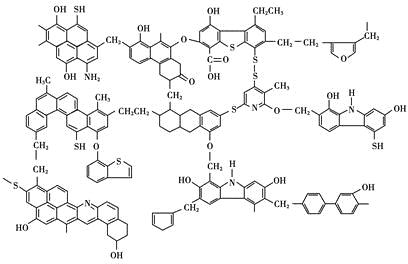
回答下列问题:
(1)从煤的结构模型来看,煤是工业上获得____________的重要来源。
(2)我国大约70%的煤是直接用于燃烧的。从煤的结构模型来看,在提供热量的同时产生大量的____________、____________等气体物质,造成严重的大气污染。
(3)“型煤”技术不仅可以减少87%的废气排放量,烟尘排放量也可减少80%,致癌物苯并[α]芘的排放量也减少,同时节煤20%~30%。“型煤”技术的原理是利用固硫剂在燃烧过程中生成稳定的硫酸盐。某“型煤”生产厂利用石灰石作固硫剂,试用化学方程式表示其固硫过程________________、________________。
(4)为了解决煤燃烧所造成的污染问题和提高煤的利用价值,煤资源的综合利用方法还有____________、____________、____________等。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,所设计的装置如下图所示:
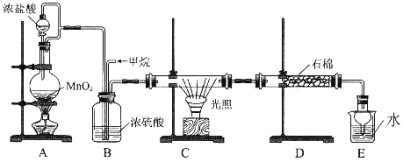
(1)最简单烷烃的空间结构为_______________。
(2)写出装置C中生成一氯甲烷的化学方程式:__________,该反应类型为:_________。
(3)D中石棉上吸附着潮湿的KI粉末,其作用是_________________________。
(4)若题目中甲烷与氯气的体积之比为1∶1,两者反应则得到的产物有____种,其中常温下为气态的有机产物的化学式为:________。
(5)将0.4molCH4与Cl2发生取代,测得4种有机取代物的物质的量相等,则消耗的氯气的物质的量是______________。
(6)烃A为甲烷的同系物,A中有12个氢原子,写出A的同分异构体中,含4个-CH3的结构简式: _________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com