
【题目】有两种新型的应用于液晶和医药的材料W和Z,可用以下路线合成。
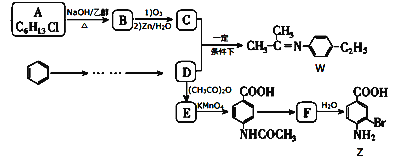
已知以下信息:
① (R1、R2、R3、R4为氢原子或烷烃基)
(R1、R2、R3、R4为氢原子或烷烃基)
②1molB经上述反应可生成2molC,且C不能发生银镜反应
③![]() (易被氧化)
(易被氧化)
④![]() +CH3-CH=CH2
+CH3-CH=CH2 ![]()
请回答下列问题:
(1)化合物A的结构简式____________,A→B的反应类型为_______________。
(2)下列有关说法正确的是____________(填字母)。
A.化合物B中所有碳原子不在同一个平面上
B.化合物W的分子式为C11H16N
C.化合物Z的合成过程中,D→E步骤为了保护氨基
D.1mol的F最多可以和4 molH2反应
(3)C+D→W的化学方程式是________________________。
(4)写出同时符合下列条件的Z的所有同分异构体的结构简式:_____________________。
①遇FeCl3溶液显紫色;
②红外光谱检测表明分子中含有![]() 结构;
结构;
③1H-NMR谱显示分子中含有苯环,且苯环上有两种不同化学环境的氢原子。
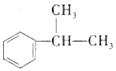
(5)设计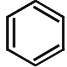 →D合成路线(用流程图表示,乙烯原料必用,其它无机过剂及溶剂任选)______________。
→D合成路线(用流程图表示,乙烯原料必用,其它无机过剂及溶剂任选)______________。
示例:CH3CHO ![]() CH3COOH
CH3COOH ![]() CH3COOCH2CH3
CH3COOCH2CH3
【答案】(CH3)2CH-CCl(CH3)2 消去反应 C ![]()
![]() 、
、![]()
![]()
【解析】
A的分子式为C6H13Cl,为己烷的一氯代物,在氢氧化钠醇溶液、加热条件下发生消去反应得到B为烯烃,1mol B发生信息①中氧化反应生成2molC,且C不能发生银镜反应,B为对称结构烯烃,且不饱和C原子没有H原子,故B为(CH3)2C=C(CH3)2,C为![]() ,逆推可知A为(CH3)2CH-CCl(CH3)2。由W
,逆推可知A为(CH3)2CH-CCl(CH3)2。由W![]() 进行逆推,可推知D为
进行逆推,可推知D为![]() ,由E后产物结构,可知D与乙酸酐发生取代反应生成E,故E为
,由E后产物结构,可知D与乙酸酐发生取代反应生成E,故E为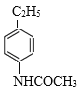 ,然后E发生氧化反应。对、比F前后物质结构,可知生成F的反应发生取代反应,而后酰胺发生水解反应又重新引入氨基,则F为
,然后E发生氧化反应。对、比F前后物质结构,可知生成F的反应发生取代反应,而后酰胺发生水解反应又重新引入氨基,则F为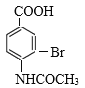 ,D→E步骤为了保护氨基,防止被氧化。
,D→E步骤为了保护氨基,防止被氧化。
根据上述分析可知:A为(CH3)2CH-CCl(CH3)2,B为(CH3)2C=C(CH3)2,C为![]() ,D为
,D为![]() ,E为
,E为 ,F为
,F为 。则
。则
(1)根据上述分析可知,化合物A的结构简式为:(CH3)2CH-CCl(CH3)2,A与NaOH的乙醇溶液在加热时发生消去反应,产生B:(CH3)2C=C(CH3)2,乙醇A→B的反应类型为:消去反应;
(2)A.化合物B为(CH3)2C=C(CH3)2,可看作是乙烯分子中4个H原子分别被4个-CH3取代产生的物质,由于乙烯分子是平面分子,4个甲基C原子取代4个H原子的位置,在乙烯分子的平面上,因此所有碳原子处于同一个平面,A错误;
B.由W的结构简式可知化合物W的分子式为C11H15N,B错误;
C.氨基具有还原性,容易被氧化,开始反应消耗,最后又重新引入氨基,可知D→E步骤为了保护氨基,防止被氧化,C正确;
D.物质F为 ,苯环能与氢气发生加成反应,1mol的F最多可以和3molH2反应,span>D错误,故合理选项是C;
,苯环能与氢气发生加成反应,1mol的F最多可以和3molH2反应,span>D错误,故合理选项是C;
(3)C+D→W的化学方程式是:![]() ;
;
(4)Z的同分异构体满足:①遇FeCl3溶液显紫色,说明含有酚羟基;②红外光谱检测表明分子中含有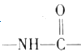 结构;③1HNMR谱显示分子中含有苯环,且苯环上有两种不同化学环境的氢原子,说明分子结构对称,则对应的同分异构体可为
结构;③1HNMR谱显示分子中含有苯环,且苯环上有两种不同化学环境的氢原子,说明分子结构对称,则对应的同分异构体可为![]() 、
、![]() ;
;
(5)由信息④可知,苯与乙烯发生加成反应得到乙苯![]() ,然后
,然后![]() 与浓硝酸、浓硫酸在加热50℃~60℃条件下得到对硝基乙苯
与浓硝酸、浓硫酸在加热50℃~60℃条件下得到对硝基乙苯![]() ,最后
,最后![]() 与Fe在HCl中发生还原反应得到对氨基乙苯
与Fe在HCl中发生还原反应得到对氨基乙苯![]() ,故合成路线流程图为:
,故合成路线流程图为:![]() 。
。


 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:
【题目】下图中A为278g/mol。B、D、E、F、G是氧化物且B为红棕色固体,F、K是氢化物,C、H是日常生活中最常见的金属单质,J是黄绿色气体。O是白色沉淀(图中部分反应物和生成物没有列出)。

(1)写出A、G、L的化学式A______________:G: _______________,L:______________。
(2)反应②的化学方程式 ________________________________________________。
(3)写出反应M→L的离子方程式为________________________________________。
(4)若将O敞口久置,变质过程中的现象为___________________________________,发生的化学方程式为__________________________________________________。
(5)向M溶液中投入与M等物质的量的Na2O2,反应的离子方程式是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请将正确的下列变化的序号填在对应的横线上:①碘的升华;②二氧化碳溶于水;③氯化钠溶于水;④烧碱熔化;⑤氯化氢溶于水;⑥氯化铵受热分解。
(1)化学键没有被破坏的是________;仅发生离子键破坏的是________;
(2)即发生离子键破坏、又发生共价键破坏的是________;
(3)N2的电子式为________;Na2O2的电子式为________;CO2的电子式为________。
(4)写出下列物质的形成过程。
HCl ___________;NaCl ______________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计实验以探究元素性质的递变规律,实验装置如图所示.

实验Ⅰ:根据元素最高价含氧酸的酸性强弱探究元素非金属性递变规律.
已知A装置的烧瓶里装有大理石,分液漏斗里装有稀HNO3,B装置中装有饱和碳酸氢钠溶液,装置C中装有Na2SiO3溶液,试回答:
(1)A中反应的离子方程式为 ,C中可观察到的现象是 .
(2)B装置的作用是 .
(3)根据实验现象推知,碳酸、硝酸、硅酸的酸性强弱顺序是 ,由此得出碳、硅、氮三种元素非金属性的强弱顺序是 .
实验Ⅱ:已知常温下高锰酸钾与浓盐酸混合可产生氯气,利用该装置探究氯和溴元素的非金属性强弱.
(4)写出B装置中发生反应的离子方程式: .
(5)C装置的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是课外活动小组设计的用化学电源使LED灯发光的装置。下列说法正确的是
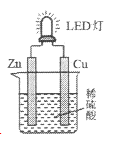
A. 溶液中的SO42-向铜极移动
B. 锌片为原电池的负极,发生还原反应
C. 如果将稀硫酸换成柠檬汁,导线中不会有电子流动
D. 铜片表面有气泡生成,发生的反应为:2H++2e-=H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,有关说法正确的是
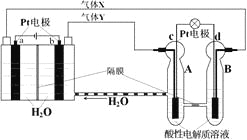
A. 转移0.1mol电子时,a电极产生标准状况下O2 1.12L
B. b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH-
C. c电极上进行还原反应,B池中的H+可以通过隔膜进入A池
D. d电极上发生的电极反应是:O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】注意分析下列两条信息,它们可能有助于你解答下面的推断题:
①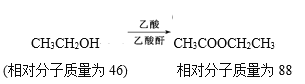
②有机化合物分子中,同一个碳原子上连接两个羟基的结构是不稳定的,易自动失去一分子水,如
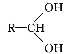
![]()
![]() +H2O(R—代表烃基)
+H2O(R—代表烃基)
现有只含C、H、O三种元素的化合物A~F,它们的某些有关信息已注明在下面的方框内。
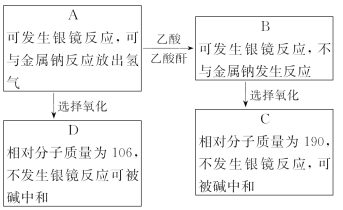
请推断出化合物A、B、C、D的结构简式。
A______________,B______________,C______________,D______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究氮、氯等单质及其化合物的反应有重要意义。
(1)科学家研究在一定条件下通过下列反应制备NH3:
![]()
①在其他条件相同时,反应中NH3的体积分数(a)在不同温度下随反应时间(t)的变化如图。该反应的平衡常数表达式K=______,该反应中的![]() ____0(填“>”“<”或“=”)。
____0(填“>”“<”或“=”)。
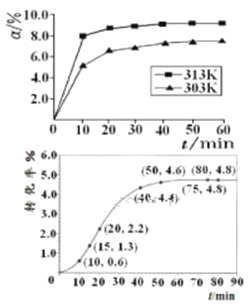
②某温度下,在2L容积不变的密闭容器中加入1molN2和6molH2O(1)发生反应,N2转化率随时间(t)变化如图。15-20min内,v(NH3)=____。若其他条件不变,在图中画出使用催化剂后N2的转化率随反应时间变化的曲线示意图_______。
(2) 25℃时,某同学将0.lmol![]() 盐酸与0.2 mol
盐酸与0.2 mol![]() 氨水等体积混合,所得混合溶液pH______7(填“>”“<”或“=”,下同),混合溶液中c(NH4+)______c(NH3
氨水等体积混合,所得混合溶液pH______7(填“>”“<”或“=”,下同),混合溶液中c(NH4+)______c(NH3![]() H2O)(25℃时,NH3.H2O的电离常数
H2O)(25℃时,NH3.H2O的电离常数![]() )
)
(3) 25℃时,向0.lmol![]() 的MgCl2溶液中逐滴加入适量0.lmol
的MgCl2溶液中逐滴加入适量0.lmol![]() 氨水,有白色沉淀生成,向反应后的浊液中,继续加入0.lmol
氨水,有白色沉淀生成,向反应后的浊液中,继续加入0.lmol![]() 的FeCl3溶液,观察到的现象是______ ;上述过程中发生的所有反应的离子方程式为______。(25℃时,
的FeCl3溶液,观察到的现象是______ ;上述过程中发生的所有反应的离子方程式为______。(25℃时,![]() ,
,![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子中,各分子的空间构型、中心原子的杂化方式以及孤电子对数均正确的是
选项 | 分子 | 空间构型 | 杂化方式 | 孤电子对数 |
A | NH3 | 平面三角形 | sp3杂化 | N含有一对孤电子对 |
B | CCl4 | 正四面体 | sp3杂化 | C不含有孤电子对 |
C | H2O | V形 | sp2杂化 | O含有两对孤电子对 |
D | CO32- | 三角锥形 | sp3杂化 | C含有一对孤电子对 |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com