

| A. | 吸热反应 | B. | 放热反应 | C. | 无热效应 | D. | 无法判断 |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一次性塑料袋使用方便又经济,应大力提倡生产和大量使用 | |
| B. | 推广利用太阳能、风能,缓解温室效应 | |
| C. | 采用焚烧的方法处理农作物秸秆和垃圾 | |
| D. | 大力开采金属矿物资源,保障金属材料的使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在该1体积盐酸中加入2体积水 | |
| B. | 将该1体积盐酸加水冲稀到3体积 | |
| C. | 将该盐酸与pH=12的氢氧化钠溶液以1:9的体积比混合 | |
| D. | 取该1体积盐酸加100体积水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、Na+、NO3-、Cl- | B. | NH4+、K+、HCO3-、OH- | ||
| C. | Na+、Al3+、AlO2-、Cl- | D. | K+、Mg2+、SO42-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
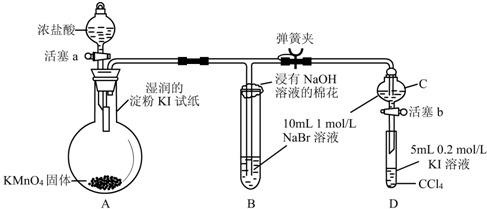
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蓄电池放电时,每消耗0.1molPb,共生成0.1mol PbSO4 | |
| B. | 电解硫酸钠溶液时的阳极反应式为:4OH--4e-=2H2O+O2↑ | |
| C. | 电解后,硫酸钠溶液中有晶体析出,但c(Na2SO4)会变小 | |
| D. | 蓄电池放电一段时间后其电解液中H2SO4的浓度、密度都变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10℃时,1LpH=1.0的H2SO4溶液中含H+为0.1NA | |
| B. | 常温下,14g的146C含中子数目为6NA | |
| C. | 标况下,11.2LNO与11.2LO2混合,原子总数小于2NA | |
| D. | 0.1mol苯乙烯含碳碳双键为0.4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com