
【题目】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:

据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是______________;
(2)溶液E所含物质是混合物,其化学式分别为___________、______________;
(3)反应②的离子方程式为______________________________ ;
(4)反应③的离子方程式为______________________________ 。
【答案】 过滤 K2SO4 (NH4)2SO4 Al3++3NH3.H2O=Al(OH)3↓+3NH4+ AlO2- + H+ + H2O= Al(OH)3↓
【解析】某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,加水后经过滤分离可得溶液KAl(SO4)2和Al2O3、Fe2O3沉淀混合物C,加入NaOH溶液,NaOH和Al2O3反应生成NaAlO2,过滤后得到NaAlO2溶液,沉淀D为Fe2O3,加入盐酸得到FeCl3,NaAlO2溶液中加入适量盐酸,反应生成Al(OH)3和NaCl,Al(OH)3加热分解生成B为Al2O3,溶液E为K2SO4和(NH4)2SO4混合物;(1)难溶性固体和溶液采用过滤方法分离;(2)硫酸铝钾溶液与氨水混合,生成氢氧化铝沉淀,得到K2SO4、(NH4)2SO4两种盐溶液;(3)铝离子和一水合氨反应生成氢氧化铝沉淀;(4)偏铝酸根离子与适量盐酸反应生成氢氧化铝沉淀。
某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,加水后经过滤分离可得溶液KAl(SO4)2和Al2O3、Fe2O3沉淀混合物C,加入NaOH溶液,NaOH和Al2O3反应生成NaAlO2,过滤后得到NaAlO2溶液,沉淀D为Fe2O3,加入盐酸得到FeCl3,NaAlO2溶液中加入适量盐酸,反应生成Al(OH)3和NaCl,Al(OH)3加热分解生成B为Al2O3,溶液E为K2SO4和(NH4)2SO4混合物;
(1)难溶性固体和溶液采用过滤方法分离,Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是过滤;正确答案:过滤。
(2)硫酸铝钾溶液与氨水混合,铝离子与一水合氨反应生成氢氧化铝沉淀,得到的溶液中溶质为K2SO4和(NH4)2SO4;正确答案:K2SO4、(NH4)2SO4。
(3)铝离子和一水合氨反应生成氢氧化铝沉淀,离子方程式为Al3++3NH3H2O═Al(OH)3↓+3NH4+;正确答案:Al3++3NH3H2O═Al(OH)3↓+3NH4+。
(4)偏铝酸根离子与适量盐酸反应生成氢氧化铝沉淀,离子方程式为:AlO2- + H+ + H2O= Al(OH)3↓;正确答案:AlO2- + H+ + H2O= Al(OH)3↓。


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在一容积不变的密闭容器中发生的可逆反应2X(g)![]() Y(g)+Z(g),达到反应限度的标志是
Y(g)+Z(g),达到反应限度的标志是
①X的分解速率与X的生成速率相等 ②反应容器中压强不再变化
③X、Y、Z的浓度不再变化 ④单位时间内生成1molY的同时生成1molZ
A.①③ B.②③ C.①② D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.同周期元素中,ⅠA族元素的原子半径最小
B.仅由非金属元素不可能形成离子化合物
C.目前使用的元素周期表中,最长的周期含有32种元素
D.凡是有化学键断裂的过程一定发生了化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组研究铝土矿中Al2O3的含量。已知铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:
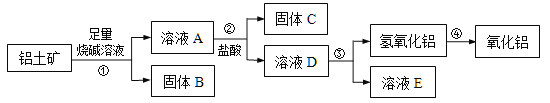
(1)固体B的主要用途有(写出1条即可)________________。
(2)第①步,向铝土矿中加入足量烧碱溶液后,发生反应的离子方程式是________________________________;_______________________________________;
第③步中,用足量氨水制氢氧化铝的化学方程式是________________________________。
(3)将实验过程中所得固体精确称量,课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,则该铝土矿中Al2O3的质量分数是__________。(保留一位小数)
(4)工业上制取AlCl3用Al2O3与C、Cl2在高温条件下反应,生成两种化合物,其中一种是还原性气体且有毒性,该反应的化学方程式是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某周期第ⅡA族元素的原子序数为x,则同周期的第ⅣA族元素的原子序数为( )
A.只能是x+2B.可能是x+8或x+18
C.可能是x+13D.可能是x+2或x+12或x+26
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】P、S、Cl最高正价依次增大,原因是( )
A. P、S、Cl都是非金属 B. 电子层数不同
C. P、S、Cl原子半径依次减小 D. P、S、Cl最外层电子数依次增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)改善空气质量、保护水土资源是实现美丽中国的基础。
①下列气体的排放会导致酸雨形成的是________(填字母,下同)。
a. CH4 b. CO c. SO2
②下列处理废水的方法属于中和法的是________。
a. 用熟石灰处理废水中的酸
b. 用臭氧处理废水中的氰化物
c. 用铁粉回收废水中的铜
③下列做法会造成土壤重金属污染的是________。
a. 作物秸杆露天焚烧
b. 废干电池就地填埋
c. 废旧塑料随意丢弃
(2)新鲜牛肉含蛋白质、脂肪、糖类、维生素A、维生素C、钙、铁等,其中:
①属于人体所需微量元素的是________。
②属于脂溶性维生素的是________。
③可为人体提供能量的是________、________和________。
(3)材料的发展与应用促进了人类社会的进步。
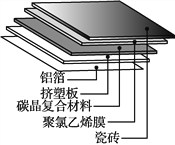
①碳晶地暖环保、节能、安全,其构造如图所示。其中属于金属材料的是________;属于硅酸盐材料的是________;属于高分子材料的是挤塑板和________。
②吸附材料具有多孔、表面积大的特点。活性炭吸附NO2的过程中,会伴有C与NO2的反应,产物为两种常见无毒气体。写出该反应的化学方程式:_________________________________________。
③LiMn2O4是锂离子电池的一种正极材料,可通过MnO2与Li2CO3煅烧制备,同时还生成CO2和一种单质。写出该反应的化学方程式:_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种微粒。已知:
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④D微粒有18个电子,当失去2个电子后显电中性;
⑤E微粒不带电,原子核中只有一个质子。
请回答:
(1)写出这五种微粒的符号:A_______,B_______,C_______,D______,E_______。
(2)B微粒的结构示意图________,D微粒的结构示意图_________。
(3)A的单质与EB溶液反应的离子方程式:_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com