
| A、将水沿烧杯内壁缓缓加入浓硫酸中,用玻璃棒不断搅拌 |
| B、实验室制取氯气时,尾气用碱液吸收 |
| C、金属钠、镁着火时,可用泡沫灭火器来灭火 |
| D、夜间厨房发生煤气泄漏时,应立即开灯检查煤气泄漏的原因,然后打开所有的门窗通风 |


科目:高中化学 来源: 题型:
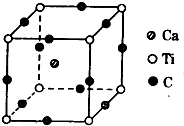 短周期元素A、B、C、D,A元素的原子最外层电子排布式为ms1,B元素的原子价电子排布式为ns2np2,C元素位于第二周期且原子中p亚层与所有s亚层电子总数相等,D元素原子的L层的p亚层中有3个未成对电子.
短周期元素A、B、C、D,A元素的原子最外层电子排布式为ms1,B元素的原子价电子排布式为ns2np2,C元素位于第二周期且原子中p亚层与所有s亚层电子总数相等,D元素原子的L层的p亚层中有3个未成对电子.查看答案和解析>>
科目:高中化学 来源: 题型:
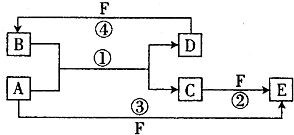
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、农作物收获后,就地焚烧秸秆,增加土壤中钾肥含量 |
| B、厨房中燃气泄漏,立即打开抽油烟机排气 |
| C、硝酸是重要的工业原料,可用于制造炸药 |
| D、高纯硅可用于制作光导纤维,光导纤维遇强碱会“断路” |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)=2c(S2-) |
| B、c(OH-)=c (H+)+c (HS-)+2c (H2S) |
| C、c(Na+)>c(S2-)>c (HS-)>c (OH-) |
| D、c(Na+)+c (H+)=2c (S2-)+c (HS-)+c (OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子序数大小:X>Y |
| B、Xm+和Yn-离子半径大小:Yn-<Xm+ |
| C、在周期表中X、Y在不同周期 |
| D、在周期表中X、Y的族序数之差为:8-(m+n) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容器里P、Q、R、S四种物质共存 |
| B、单位时间内消耗n mol P同时生成n mol S |
| C、容器内气体压强、密度不随时间变化 |
| D、容器里Q、R的体积分数不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、在稀氨水中通入过量CO2:NH3?H2O+CO2=N
| ||||
| B、少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO | ||||
C、向Ba(OH)2溶液中加入少量的NaHSO3溶液2HS
| ||||
| D、氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-=CaSO4↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com