
(12��) ��������11����ѧ��ѧ���������ʣ���һ�������¿���ʵ����ͼ��ʾ��ת����ϵ��ͼ��ijЩ��Ӧ����������Ѿ���ȥ��
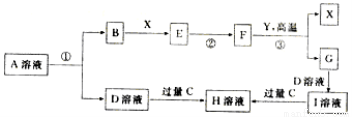
��֪��AΪ����Ԫ����ɵĻ��������ɫ��Ӧ����ɫ�ܲ����۲쵽Ϊ��ɫ��BΪ���ʣ���һ���ж����壻��Ӧ�ٵ��������ö��Ե缫��⣻��Ӧ�ڵ������ǽ�E��ˮ��Һ�������ɡ����գ�YΪ����������F�н���Ԫ�أ�+3�ۣ���������Ϊ70%��CΪ����22���ӵ������
�ش��������⣺
��1��D�ĵ���ʽΪ____��H�Ļ�ѧʽΪ ��
��2����Ӧ�۵Ļ�ѧ����ʽΪ ������Cͨ��I��Һ�з�����Ӧ�����ӷ���ʽΪ ��
��3��ָ��G��һ����;�� ��
��4����һ������Bͨ�뵽����l mol XBr2����Һ�У�����1/3��Brһ����������ͨ���B�ڱ�״���µ����Ϊ L(����һλС��)��
��5����ͬѧ˵���������������������x����������Һ�������ɺ�õ��Ĺ��������E�������ɺ�õ��Ĺ�������ͬ�ġ������˵���Ƿ���ȷ�� �����ȷ������ȷ������������ ��
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������¼��8���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��ɫ��Һ�������������е������֣�H+��NH4+��Fe3+��Ba2+��Al3+��CO32�C��Cl�C��OH�C��NO3�C�������Һ�м������ۣ�ֻ�ų�H2������Һ���ܴ������ڵ����������
A��3�� B��4�� C��5�� D��6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A����Ҫ���ȷ��ܷ����ķ�Ӧһ�������ȷ�Ӧ
B�����ȷ�Ӧ�ڳ���������һ����������
C����Ӧ�����Ȼ��Ƿ��ȵģ�Ҫ����Ӧ����������������������Ĵ�С
D�����ȵ�̿�������̼�ķ�ӦΪ���ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ������ѧ�ڵ�һ��ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��Na+����Һ�п��ܺ���Al3+��NH4+��Fe3+��CO32-�� I-��SO32-��ȡ�����μ�������ˮ�������ݲ�������������Һ�м�BaCl2��Һ����۾�������Ϊȷ������Һ����ɣ�������е�ʵ����
A��ȡ�����μ����軯����Һ
B��ȡ������������ŨNaOH��Һ���ȣ���ʪ��ĺ�ɫʯ����ֽ��������
C��ȡ������ε�������������Һֱ������
D��ȡ����������������ȣ�ʪ���Ʒ����ֽ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ν�Ͻ𣬾��Dz�ͬ�ֽ���(Ҳ����һЩ�ǽ���)������״̬���γɵ�һ���ۺ�������������ֽ������ۡ��е㣬�ж����в����γɺϽ����
Na | Cu | Al | Fe | |
�۵�/�� | 97.5 | 1 083 | 660 | 1 535 |
�е�/�� | 883 | 2 595 | 2 200 | 3 000 |
A��Cu��Al B��Fe��Cu C��Fe��Na D��Al��Na
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������һ�β������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�谢���ӵ�����ΪNA��������˵����ȷ����
A��100 g 98%��Ũ�����к���ԭ������Ϊ4NA
B�����³�ѹ�£�18g��ˮ(D2O)�������ĵ�����Ϊ10 NA
C�����³�ѹ�£�4��6 g NO2���庬��0��3 NA��ԭ��
D�������£�2��7g��ƬͶ��������Ũ�����У�������SO2��������Ϊ0��3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ��ˮ�и����ϵ�һ�μ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ҵ�Ͻ�Na2CO3��Na2S��1:2�����ʵ���֮�������Һ����ͨ��SO2������ȡNa2S2O3��ͬʱ�ų�CO2���ڸ÷�Ӧ��
A����Ԫ���ڴ˹����н�����ԭ
B���������뻹ԭ�������ʵ���֮��Ϊ1:2
C��ÿ����1molNa2S2O3��ת��4mo l����
D����ͬ�����£�ÿ����10m3SO2�ͻ�ų�2.5m3CO2[
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ����Ͽ�и߶���ѧ����ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ں����ܱ������н���N2��3H2 2NH3��Ӧ����ʼʱN2��H2�ֱ�Ϊ10 mol ��30 mol�����ﵽƽ��ʱ��N2��ת����Ϊ30%������NH3��Ϊ��ʼ��Ӧ���Ӧ������������Ӧ��ͬʱ��Ҫʹ�䷴Ӧ�ﵽƽ��ʱ����ɳɷֵ����ʵ���������ǰ����ͬ����NH3����ʼ���ʵ���������ת������ȷ����
2NH3��Ӧ����ʼʱN2��H2�ֱ�Ϊ10 mol ��30 mol�����ﵽƽ��ʱ��N2��ת����Ϊ30%������NH3��Ϊ��ʼ��Ӧ���Ӧ������������Ӧ��ͬʱ��Ҫʹ�䷴Ӧ�ﵽƽ��ʱ����ɳɷֵ����ʵ���������ǰ����ͬ����NH3����ʼ���ʵ���������ת������ȷ����
A��40 mol 35% B��20 mol 30%
C��20 mol 70% D��10 mol 50%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��̫ԭ���и߶��ϵ�һ�ܿ����ƻ�ѧ�Ծ��������棩 ���ͣ������
��1������Һ��������Ҫ�ɷ�֮һ�Ƕ��飨C4H10������1kg������ȫȼ�����ɶ�����̼��Һ̬ˮʱ���ų�����Ϊ5��104kJ����д����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ ��
��2����ѧ������̫���ֽܷ�ˮ���ɵ������ڴ����������������̼��Ӧ���ɼ״�����������ֱ���Լ״�Ϊȼ�ϵ�ȼ�ϵ�ء���֪H2(g)��CO(g)��CH3OH(l)��ȼ���Ȧ�H�ֱ�Ϊ��285��8 kJ/mol����283��0 kJ/mol�ͣ�726��5 kJ/mol����ش��������⣺
����̫���ֽܷ�10 molˮ���ĵ������� kJ��
�ڼ״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ ��
���о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���壬��֪��
2SO2(g)��O2(g) = 2SO3(g) ��H����196��6 kJ/mol
2NO(g)��O2(g) = 2NO2(g) ��H����113��0 kJ/mol
��ӦNO2(g)��SO2(g)=SO3(g)��NO(g)�Ħ�H�� kJ/mol��
��3����˹�����������Ϳ�ѧ�о����к���Ҫ�����壮��Щ��Ӧ�ķ�Ӧ����Ȼ��ֱ�Ӳ�ã�����ͨ����ӵķ����ⶨ���ָ�������3���Ȼ�ѧ��Ӧ����ʽ��
Fe2O3��s��+3CO��g���T2Fe��s��+3CO2��g����H=-24��8kJ•mol-1
3Fe2O3��s��+CO��g���T2Fe3O4��s��+CO2��g����H=-47��4kJ•mol-1
Fe3O4��s��+CO��g���T3FeO��s��+CO2��g����H=+640��5kJ•mol-1
д��CO��g����ԭFeO��s���õ�Fe��s�����CO2��g�����Ȼ�ѧ��Ӧ����ʽ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com