
分析 (1)镓是31号元素,其原子核外有31个电子,根据构造原理书写其核外电子排布式;
(2)一般来说,晶体熔沸点:原子晶体>离子晶体>分子晶体,对于离子化合物来说,决定于离子晶体,所带的电荷数越多、半径越小键能越大,熔点越高,据此分析.
解答 解:(1)镓是31号元素,其原子核外有31个电子,根据构造原理知其核外电子排布式1s22s22p63s23p63d104s24p1或[Ar]3d104s24p1,
故答案为:1s22s22p63s23p63d104s24p1或[Ar]3d104s24p1;
(2)一般来说,晶体熔沸点:原子晶体>离子晶体>分子晶体,所以②金刚石为原子晶体熔点最高,③干冰为分子晶体熔点最低,而①氧化镁 和④氯化钾都为离子晶体,其中氧化镁中离子所带电荷数多、半径小,所以熔点①氧化镁 大于④氯化钾,则熔点由高到低排列②>①>④>③;
故答案为:②>①>④>③,依据原子晶体>离子晶体>分子晶体,对于离子化合物来说,决定于离子晶体,所带的电荷数越多、半径越小键能越大,熔点越高.
点评 本题考查了原子核外电子排布式的书写、晶体熔点的判断等知识点,抓住晶体类型与熔沸点的关系来分析解答,难度不大,注意基础知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | 淀粉和纤维素 | B. | 蔗糖和麦芽糖 | ||
| C. | 分子式为C4H6和C5H8的烃 | D. | 分子式为C4H10和C20H42的烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
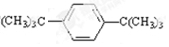 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,则原有机物一定是( )
,则原有机物一定是( )| A. | 1,3-丁二烯 | B. | 2-甲基-1,3-丁二烯 | ||
| C. | 2-丁炔 | D. | 1,4-二氯-2-甲基-2-丁烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 | |
| B. | 金属与酸的反应 | |
| C. | 甲烷在氧气中的燃烧反应 | |
| D. | 锌粒与稀硫酸的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
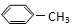 分子结构的下列叙述中,正确的是( )
分子结构的下列叙述中,正确的是( )| A. | 七个碳原子可能不在同一平面上 | B. | 具有单键和双键两种键 | ||
| C. | 八个氢原子不可能都在同一平面上 | D. | 最多可能有5个C原子在一条直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 阅读下列信息,完成下列各题
阅读下列信息,完成下列各题查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com