
����Ŀ��I.��ͼ�ס��ҡ�����Ϊ��֤ͭ��Ũ���ᷴӦ��װ�ã�

(1)�ס��ҡ�������װ���й�ͬ�����Ļ�ѧ����ʽ��___________________��
(2)�ͼ�װ����ȣ���װ�õ��ŵ���
��________________________________________________��
��_______________________________________________��
(3)Ϊ�˽�һ����֤NO2��ˮ�ķ�Ӧ��ijѧ������˱�װ�á�ʵ��ʱ�ȹرջ���c���ٴ���a��b������ʹNO2����������Թܣ�������������Թܺ�ͭ˿��������Һ���롣��ʹ�ձ��е�ˮ������Թܣ�Ӧ����β���_________________��
(4)���Թ��е�NO2��ˮ��ַ�Ӧ��������Һ���ʵ���Ũ�ȵ����ֵ��_____mol/L (�����������״������)��
II.֤��±��Ԫ�صķǽ�����ǿ����ijС������ͼ��ʾװ�ý���ʵ��(�г���������ȥ�������Լ��)

ʵ����̣���.���ɼУ�����a���μ�Ũ���ᡣ
��.��B��C�е���Һ����Ϊ��ɫʱ���н����ɼС�
��.��B����Һ�ɻ�ɫ��Ϊ�غ�ɫʱ���رջ���a�� ��.����
(1)��֤������������ǿ�ڵ��ʵ��������________________________________________��
(2)B����Һ������Ӧ�����ӷ���ʽ��____________________________________��
(3)Ϊ��֤���������ǿ�ڵ⣬���� �� �IJ�����������__________________��
(4)�ȡ��塢�ⵥ�ʵ�������������ԭ��ͬ����Ԫ�ش��ϵ��£�ԭ�Ӱ뾶��________���õ���������________��
���𰸡�Cu��4HNO3(Ũ)��Cu(NO3)2��2NO2����2H2O ���Կ��Ʒ�Ӧ�ķ�����ֹͣ ���ն����������壬��ֹ������Ⱦ �ȹر�b���ٹر�a��Ȼ���c��������ס�Թܢ� 1/22.4 ���۵⻯����ֽ���� 2Br��+Cl2��Br2+2Cl�� ����b��������C����Һ����D�У��رջ���b��ȡ��D����ֹ�����Ȼ�̼����Һ��Ϊ�Ϻ�ɫ ���� ����
��������
I.��1��ͭ��Ũ���ᷴӦ��������ͭ������������ˮ���ݴ���д��
��2�����ݷ�Ӧ�ɿ��ƣ���ʱ����ֹͣ�Լ��Ƿ����������Ⱦ�������
��3����ʹ�ձ��е�ˮ������Թܣ���Ҫ�ö���������ˮ�Ӵ����ݴ��жϣ�
��4��������������ˮ���������NO���ݴ˼��㡣
��.װ��A�Ǹ����������Ũ�������������������͵⻯�ط�Ӧ���ɵ��ʵ⣬������������ɫ�����ɵ�����ͨ��װ��B�к��廯�Ʒ�Ӧ���ɵ����壬֤������������ǿ���壬��ͨ��װ��C�ų����������û����ʵ����ţ��ݴ˽��
I.��1���ס��ҡ�������װ���й�ͬ�����ķ�Ӧ��Ũ������������ͭ����Ӧ�Ļ�ѧ����ʽ��Cu��4HNO3(Ũ)��Cu(NO3)2��2NO2����2H2O��
��2���ͼ�װ����ȣ���װ����ʹ��Ӧ�ɿ��ƣ�ͨ���ƶ�ͭ˿����ʱ����ֹͣ��Ӧ���Ƚ�ʡ��Դ�ֱ����˻�����ͬʱ���ղ����Ķ����������壬��ֹ������Ⱦ��
��3��Ϊ��NO2����������Թܣ��ȹرջ���c���ٴ���a��b��Ϊ���ö���������ˮ��ֽӴ�������Ӧ��Ӧ�ȹر�b���ٹر�a��Ȼ���c��������ס�Թܢڼ��ɣ�
��4�����Թܵ��ݻ���VL������ݷ���ʽ3NO2��H2O��2HNO3��NO��֪������Һ���ʵ���Ũ�ȵ����ֵ��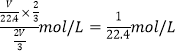 ��
��
��.��1�������������Ũ�������������������ѵ⻯������Ϊ���ʵ⣬����֤������������ǿ�ڵ��ʵ�������ǵ��۵⻯����ֽ������
��2�����ɵ�����ͨ��Bװ���а��廯������Ϊ�����壬��B����Һ������Ӧ�����ӷ���ʽ��2Br��+Cl2��Br2+2Cl����
��3������Ҫ�ų����������û����ʵ����ţ���Ϊ��֤���������ǿ�ڵ⣬���̢��IJ����������Ǵ���b��������C����Һ����D�У��رջ���b��ȡ��D����ֹ�����Ȼ�̼����Һ��Ϊ�Ϻ�ɫ��
��4���ȡ��塢�ⵥ�ʵ�������������ԭ��ͬ����Ԫ�ش��ϵ��£�ԭ�Ӱ뾶�����õ�������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��A��B��C��D��ԭ��������������B��Dͬ���壻X��Y��N�ֱ�������������Ԫ����������ɵĻ����Z������������Ԫ����ɵĻ������X��YĦ��������ͬ��YΪ����ɫ���壬��������֮���ת����ϵ��ͼ��ʾ������������ʡ�ԣ���������˵����һ����ȷ���ǣ�������
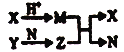
A. ��Է�������M>N���е�M>N B. �����Ӱ뾶��D>B>C>A
C. Z Ϊ Na2CO3 D. ͼ��������������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��ͭ��(Cu2S)�ɷ�����Ӧ��2Cu2S��2H2SO4��5O2===4CuSO4��2H2O���÷�Ӧ�Ļ�ԭ����________________����1 mol O2������Ӧʱ����ԭ����ʧ���ӵ����ʵ���Ϊ_________mol��
(2)���������Ļ�ѧ����ʽΪ4KAl(SO4)2��12H2O��3S===2K2SO4��2Al2O3��9SO2��48H2O���ڸ÷�Ӧ�У���ԭ����_____________��
(3)KClO3������ʵ������O2�������Ӵ�����400��ʱ�ֽ�ֻ���������Σ�����һ�����������Σ���һ���ε��������Ӹ�����Ϊ1��1��д���÷�Ӧ�Ļ�ѧ����ʽ��________________________��
(4)ʵ���ҴӺ����Һ(��H2O�⣬����CCl4��I2��I����)�л��յ⣬��ʵ��������£�
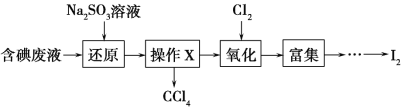
���Һ�м����Թ�����Na2SO3��Һ������Һ�е�I2��ԭΪI���������ӷ���ʽΪ_________________���ò�����I2��ԭΪI����Ŀ����________________________��
(5)��H2S�Ϳ����Ļ������ͨ��FeCl3��FeCl2��CuCl2�Ļ����Һ�з�Ӧ����S��������ת����ͼ��ʾ����ͼʾ��ת���У����ϼ۲����Ԫ����________________��
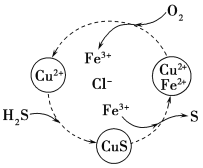
(6)NaBH4��һ����Ҫ�Ĵ������壬����ˮ��Ӧ�õ�NaBO2���ҷ�Ӧǰ��B�Ļ��ϼ۲��䣬�÷�Ӧ�Ļ�ѧ����ʽΪ________________����Ӧ����1 mol NaBH4ʱת�Ƶĵ�����ĿΪ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ�鱨���¼���������ݣ��������ݺ�������
A. ���¶ȼƲ������ƾ��ķе�Ϊ78��5��
B. ��50mL��Ͳ��ȡ23��00 mLŨ����
C. �ù㷺pH��ֽ�����ˮ��pHΪ2
D. ��������ƽ��������ͭ��ĩΪ11��70g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1.92gͭͶ��һ����ŨHNO3�У�ͭ��ȫ�ܽ⣬����������ɫԽ��Խdz�����ռ���672mL���壨���������ʢ�д����������������ˮ�У�ͨ������һ�������O2��ǡ��ʹ������ȫ����ˮ�У���ͨ��O2�����������
A. 504mL B. 168mL C. 336mL D. 224mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Fe3+��Fe2+����ʵ���˵���������(����)

A. ����ͼװ�ÿ����Ʊ�Fe(OH)2����
B. ����FeCl3��Һʱ,�Ƚ��Ȼ����������ڽ�Ũ��������,�ټ�ˮϡ�͵�����Ҫ��Ũ��
C. ��ij��Һ�еμ�KSCN��Һ,��Һ����ɫ,�μ���ˮ����Һ�Ժ�ɫ,��������ȷ����Һ�к���Fe2+
D. ��FeCl2��Һ�м�������������Ϊ�˷�ֹFe2+������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��Ϊ̽��ͭ��Ũ����ķ�Ӧ��������ͼ��ʾװ�ý����й�ʵ�顣
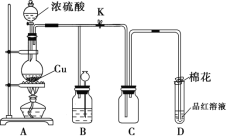
(1)װ��A�з�����Ӧ�Ļ�ѧ����ʽΪ_________________________________________��
(2)װ��B�������������������塣��D�������Ե�����ر�����K����ȥ�ƾ��ƣ����������ȵ����ã�A�����������������ʱB��������________________��B��Ӧ���õ���Һ��________(����ĸ)��
a��ˮ b������KMnO4��Һ c��Ũ��ˮ d������NaHSO3��Һ
(3)��װ��C��ʢ������KMnO4��Һ����Ӧ����Ϊ_____________________�����ָ������_____________��������ԡ���ԭ�ԡ�����
(4)װ��D���Թܿڷ��õ���Ӧ��һ����Һ��������Һ��_____________����������___________��
(5)ʵ���У�ȡһ��������ͭƬ��һ�����18 mol��L��1��Ũ�������Բ����ƿ�й��ȣ���Ӧ���ʱ��������ƿ�л���ͭƬʣ�࣬��С��ѧ��������ѧ�Ļ�ѧ֪ʶ��Ϊ����һ����������ʣ�࣬��ԭ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ֱ��ʾ�йط�Ӧ�ķ�Ӧ�����������仯�Ĺ�ϵ���ݴ��ж�����˵������ȷ����(����)
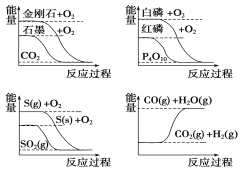
A. ���ױȺ����ȶ�
B. S(g)��O2(g)===SO2(g)����H1��S(s)��O2(g)===SO2(g)����H2������H1>��H2
C. CO(g)��H2O(g)===CO2(g)��H2(g)����H>0
D. ʯīת��Ϊ���ʯ�����ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�����ģ����ɿ�����4�����������ϵ�3����ˮ���ã�![]() ��ʽ�е�R��R�䡢R�塢R��������ͬ�Ļ�ͬ����������ȡ��������������NH��CO����Ϊ�ļ�������һ�������ġ��������ʽ��C55H70O19N10����֪��������ˮ���ֻ�õ��������ְ����
��ʽ�е�R��R�䡢R�塢R��������ͬ�Ļ�ͬ����������ȡ��������������NH��CO����Ϊ�ļ�������һ�������ġ��������ʽ��C55H70O19N10����֪��������ˮ���ֻ�õ��������ְ����

�ʣ�
��1����������ġ���_________�ģ�
��2���ö���ˮ�����_________���Ȱ��
��3���ö���ˮ�����_________���������ᡣ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com