
某元素的核素AZ X,其氯化物XCl2111mg溶于水后,加入0.1mol/L的硝酸银溶液20mL,恰好将其中的Cl-完全沉淀。已知该核素中的质子数和中子数相等。试回答下列问题:
(1)X元素的原子序数为 ,原子结构示意图为 ;
(2)用电子式表示出XCl2的形成过程 ;
(3)将X的单质放入含有酚酞的水中,现象是 ;写出该反应的化学方程式 。
科目:高中化学 来源: 题型:
铝热反应常用于冶炼高熔点的金属, 可简单认为是铝与某些金属氧化物在高温条件下发生的反应。某学习小组对铝热反应(以Al和Fe2O3反应为例)实验进行研究。
查阅数据得到Al、Al2O3、Fe、Fe2O3的熔点、沸点数据如下表所示:
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1565 |
| 沸点/℃ | 2467 | 2980 | 2750 | ┄ |
试回答下列问题:
(1)在铝热反应中金属铝表现出 性(填“氧化”或“还原”)。请判断下列金属中那一个不能由铝热反应制取 。(填序号)
①Fe ②Cr(铬) ③V(钒) ④Ca ⑤Mn
(2)某同学推测,铝热反应所得到的熔融物中应含有铁、铝两种金属。如设计一个简单的实验方案证明该熔融物中含有金属铝,则实验所需用的试剂为 ,可观察到的实验现象是 。
(3)另一同学推测铝热反应得到的熔融物中还含有Fe2O3,他设计了如下方案来验证:
取一块该熔融物投入到少量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色未变血红色,即可证明熔融物中不含有Fe2O3。则
①物质甲是 (填化学式)。
②该同学的实验方案是否合理? (填“合理”或“不合理”)。
理由:
查看答案和解析>>
科目:高中化学 来源: 题型:
将pH=1的盐酸平均分成2份,1份加适量水,另1份加入与该盐酸物质的量浓度相同的适量NaOH溶液后,pH都升高了1,则加入的水与NaOH溶液的体积比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在海水的综合利用中,海水提溴工业是一个重要组成部分,其中一种提溴的工艺是在预先浓缩并酸化的海水中,通入足量氯气,然后使生成的溴与吸收剂SO2反应转化为氢溴酸以达到富集溴元素的目的。在有关上述工艺流程的以下化学用语中,正确的是
A.用电子式表示溴化氢的形成过程为:
B.海水中Br-的电子式为:
C.海水中通入氯气时发生反应的离子方程式为:2NaBr+Cl2=Br2+2NaCl
D.氯离子的结构示意图为:
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出表示含有8个质子、10个中子、10个电子的离子的符号 。
(2)周期表中位于第8纵行的铁元素属于第 族。
(3)周期表中最活泼的非金属元素位于第 纵行 族。
(4)所含元素超过18种的周期是第 、 周期。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列实验事实:①Cr2O3固体既能溶于KOH溶液得到KCrO2溶液,又能溶于硫酸得到Cr2(SO4)3溶液;②将K2Cr2O7溶液滴加到淀粉和KI的混合溶液中,溶液变蓝;③向KCrO2溶液中滴加H2O2溶液,再酸化,可得K2Cr2O7溶液。下列判断不正确的是
A.化合物KCrO2中Cr元素为+3价 B.实验①证明Cr2O3是两性氧化物
C.实验②证明氧化性:Cr2O72->I2 D.实验③证明H2O2既有氧化性又有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学—选修3:物质结构与性质】(15分)乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。 (1) CaC2与水反应生成乙炔的反应方程式为________.
(2)比较第二周期元素C、N、O三种元素的第一电离能从大到小顺序为 ______(用元素符号表示),用原子结构观点加以解释______。
 (3)CaC中C22-与O22+互为等电子体,O22+的电子式可表示为______;1molO22+中含有的Π键数目为_______。
(3)CaC中C22-与O22+互为等电子体,O22+的电子式可表示为______;1molO22+中含有的Π键数目为_______。
(4)CaC2晶体的晶胞结构与NaCI晶体的相似(如右图所示),但CaC2
晶体中含有的中哑铃形C22-的存在,使晶胞沿一个方向拉长。CaC2晶体
中1个Ca2+周围距离最近的C22-数目为______。
(5)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基
态核外电子排布式为 _______。
(6)乙炔与氢氰酸反应可得丙烯腈(H2C

 =CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是______;分子中处于同一直线上的原子数目最多为______。
=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是______;分子中处于同一直线上的原子数目最多为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.用湿润的pH试纸测溶液的pH
B.用蒸馏法可将海水淡化为可饮用水
C.常温下浓硫酸不能盛放在铝制容器中
D.配制溶液时仰视容量瓶刻度线定容会使溶液浓度偏高
查看答案和解析>>
科目:高中化学 来源: 题型:
几种短周期元素的原子半径及主要化合价如下表:
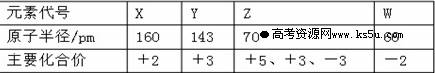
下列叙述正确的是 ( )
A.X、Y元素的金属性 X<Y
B.一定条件下,Z单质与W的常见单质直接生成ZW2
C.Y的最高价氧化物对应的水化物能溶于氨水
D.Z的气态氢化物与其最高价氧化物对应的水化物可以反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com