
【题目】请根据如下实验过程,回答相关问题:
![]()
(1)向A溶液中滴入几滴KSCN溶液后可观察到的现象是_______________________。
(2)写出反应①的化学方程式_________________________________。
写出反应②的离子方程式_________________________________。
【答案】 溶液变为血红色 Fe2O3+6HCl===2FeCl3+3H2O 2Fe3++Fe===3Fe2+
【解析】氧化铁与盐酸反应生成氯化铁和水,得到的A溶液为FeCl3溶液,加入足量铁粉,与FeCl3反应生成FeCl2,B溶液为FeCl2溶液,在B溶液中通入足量氧气的同时加入NaOH溶液,反应生成Fe(OH)3沉淀,所以C固体为Fe(OH)3。
(1). A溶液中含有Fe3+,向A溶液中滴入几滴KSCN溶液,可观察到溶液变为血红色,故答案为:溶液变为血红色;
(2). 由上述分析可知,反应①是氧化铁与盐酸反应生成氯化铁和水,化学方程式为Fe2O3+6HCl=2FeCl3+3H2O,反应②是铁粉与FeCl3反应生成FeCl2,离子方程式为2Fe3++Fe=3Fe2+,故答案为:Fe2O3+6HCl=2FeCl3+3H2O;2Fe3++Fe=3Fe2+。


科目:高中化学 来源: 题型:
【题目】为探究一溴环己烷( ![]() )与NaOH的醇溶液共热发生的是水解反应还是消去反应,甲、乙、丙三位同学分别设计如下三个实验方案:
)与NaOH的醇溶液共热发生的是水解反应还是消去反应,甲、乙、丙三位同学分别设计如下三个实验方案:
甲:向反应混合液中滴入稀硝酸中和NaOH,然后再滴入AgNO3溶液,若有浅黄色沉淀生成则可证明发生了消去反应.
乙:向反应混合液中滴入溴水,若溶液颜色很快褪去,则可证明发生了消去反应.
丙:向反应混合液中滴入酸性KMnO4溶液,若溶液颜色变浅,则可证明发生了消去反应.其中正确的是( )
A.甲
B.乙
C.丙
D.上述实验方案都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述错误的是
A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 如图所示实验可证明元素的非金属性:Cl>C>Si
C. 若X-和Y2-的核外电子层结构相同,则原子序数:X>Y
D. 在周期表中金属与非金属分界处的锗是一种优良的半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关浓硫酸和浓硝酸的叙述错误的是
A. 浓H2SO4具有吸水性,因而可作干燥剂
B. 稀硝酸中可大量含有Cu2+、Fe2+、Cl-、SO![]()
C. 浓硝酸具有强氧化性,能使铝钝化,故常用铝罐车运输冷的浓硝酸
D. 向50mL18.4mol/LH2S04溶液中加入足量的铜片并加热,充分反应后,被还原的H2S04的物质的量小于0.46mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种常见有机物分子的比例模型示意图如下,其中甲、乙、丙为烃,丁为烃的衍生物。

(1)可以鉴别甲和乙的试剂为__________;
a.稀硫酸 b.溴的四氯化碳溶液 c.水 d.酸性高锰酸钾溶液
(2)上述物质中有毒、有特殊气味,且不溶于水、密度比水小的是______(填名称),将其加入溴水中,振荡后静置,观察到的现象是______。
(3)以乙为主要原料合成乙酸,合成路线如图所示:(已知2CH3CHO+O2![]() 2CH3COOH)
2CH3COOH)
![]()
①丁生成A的化学方程式为_______________;
②如图,丁与乙酸在浓硫酸作用下发生反应,当观察到b试管中有明显现象时,停止实验。生成的有机物的结构简式为___________;试管b中的溶液是___________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资料显示:锌与浓硫酸共热除生成二氧化硫气体外,还可能产生氢气;在加热的条件下二氧化硫可被CuO氧化。为验证该反应的气体产物及性质,设计了如下图所示的实验装置(设锌与浓硫酸共热时产生的气体为X)。
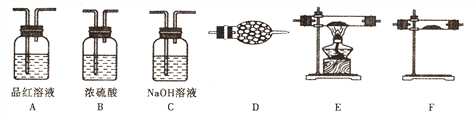
(1)上述装置的连接顺序为:气体X→A→____→A→ → → →D;
(2)反应开始后,观察到第一个装置A中的品红溶液褪色,实验结束后取适量该溶液于试管中并加热,现象为______________;
(3)装置C的作用是____,C中的NaOH溶液不能用下列____代替;
a.酸性KMnO4溶液 b.CaCl2溶液 c.饱和NaHSO3溶液
装置D的作用是____________;
(4)气体X中可能含有H2的原因是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中通入X并发生反应:2X(g)Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是( ) 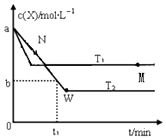
A.M点时再加入一定量的X,平衡后X的转化率增大
B.T2下,在0~t1时间内,v(Y)= ![]() mol/(L?min)
mol/(L?min)
C.M点的正反应速率v正小于N点的逆反应速率v逆
D.该反应进行到M点吸收的热量小于进行到W点放出的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列古诗词描述的场景中发生的化学反应不属于氧化还原反应的是()
A. 爆竹声中一岁除——黑火药受热爆炸
B. 蜡烛成灰泪始干——石蜡的燃烧
C. 炉火照天地,红星乱紫烟——铁的冶炼
D. 粉身碎骨浑不怕——块状的生石灰制成供人们使用的粉末状的熟石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人类较早使用的金属之一。运用所学知识,回答下列问题。
(1)鉴别Fe(OH)3胶体和FeCl3溶液的方法是_____________________________。
(2)有一铁的氧化物样品,用5mol/L盐酸140mL恰好完全溶解,所得溶液还能吸收标况下560mL氯气,Fe2+全部变成Fe3+,则该样品中Fe 和O 的个数比为_____________。
(3)某研究性学习小组用Fe2(SO4)3溶液腐蚀绝缘板上的铜,制造印刷电路板,为测定Fe2(SO4)3腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则可检出待测液中含有的金属阳离子是_____;
②验证该溶液中含有Fe2+,正确的实验方法是__________(用字母代号填)。
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+
(4)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如下方案:
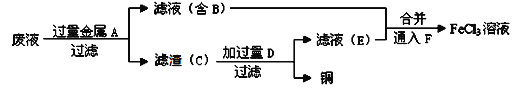
①滤渣C的主要成分的化学式为___________________________________。
②加过量D发生反应的离子方程为__________________________________。
③通入F发生反应的化学方程式为 __________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com