
【题目】已知2MOyx-+5S2-+16H+=2M2++5S↓+8H2O,则MOyx-中 M 的化合价为( )
A.+7
B.+6
C.+4
D.+3
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:
【题目】除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的的是
A. 硝基苯(硝酸) NaOH溶液 分液
B. 乙烯(二氧化硫) 酸性高锰酸钾 洗气
C. 乙酸乙酯(乙酸) NaOH溶液 蒸馏
D. 苯(苯酚) 溴水 过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气污染已成为一大公害。汽车内燃机中,汽油气化后与空气按一定比例混合进入汽缸,引擎用电火花引燃。汽油燃烧使气缸内温度迅速升高,气体体积急剧膨胀,产生压力推动活塞。燃烧时产生的有害气体通过尾气排出,从而污染大气。为简化讨论,假设汽油的成分全部为辛烷,并假设空气中氧气的体积分数为20%,其余为氮气。请回答下列问题:
(1)设辛烷气体与空气的体积比为a,要使辛烷完全燃烧,则a的最大值为_____________。
(2)若辛烷与空气的体积比大于a的最大值时,污染大气的有害气体相对增多的是______________________。
(3)若辛烷与空气的体积比小于a的最大值时,则尾气中所含污染大气的有害气体增多的是_____________,产生此气体的化学方程式是____________________________。
(4)当辛烷与空气的体积比小于a的最大值时,从能量角度来分析,有利也有弊,如其有利的因素是氧气过量,有利于汽油完全燃烧,提高能源利用率。请你举出一个不利的因素:_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料。为了分析某AlN样品(样品中的杂质不与NaOH溶液反应)中 AlN的含量,某实验小组设计了如下两种实验方案。已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。

(1)上图装置中,U形管B中所装固体为________,C中球形干燥管的作用是_______________________。
(2)关闭K1打开K2,再打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是_______________________________________。
(3)由于上述装置还存在____________缺陷,导致测定结果偏高。
【方案2】按以下步骤测定样品中AlN的纯度:
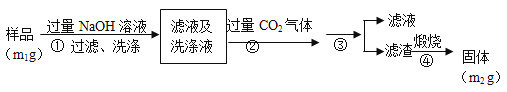
(4)步骤②生成沉淀的离子方程式为___________________。
(5)步骤③的操作中用到的主要玻璃仪器是_________。AlN的纯度是__________(用m1、m2表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
(1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。
①Mn2+基态的电子排布式可表示为 。
②NO3-的空间构型 (用文字描述)。
(2)在铜锰氧化物的催化下,CO被氧化成CO2,HCHO被氧化成CO2和H2O。
①根据等电子原理,CO分子的结构式为 。
②H2O分子中O原子轨道的杂化类型为 。
③1molCO2中含有的σ键数目为 。
(3)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,Y是X物质中含有的少量杂质,Z是除杂试剂,其中所加试剂最合理的一组是( )
X | Y | Z | |
A | NaHCO3溶液 | Na2CO3 | BaCl2溶液 |
B | FeCl3溶液 | CuCl2 | Fe |
C | Fe2O3 | Al2O3 | NaOH溶液 |
D | Na2SO4溶液 | Na2CO3 | 盐酸 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铜[xCuCO3·yCu(OH)2],呈孔雀绿颜色.又称为孔雀石,是一种名贵的矿物宝石。它与铜与空气中的氧气、二氧化碳和水蒸气等物质反应产生的物质。CuSO4溶液与Na2CO3溶液反应可以得到碱式碳酸铜,我们将对其组成进行相关探究。
[沉淀制备]
称取12. 5 g胆矾(CuSO4 5H2O)溶于87. 5mL蒸馏水中,滴加少量稀硫酸(体积可以忽略不计),充分搅拌后得到CuSO4溶液。向其中加入Na2CO3溶液,将所得蓝绿色悬浊液过滤,并用蒸馏水洗涤,再用无水乙醇洗涤,最后低溫烘干备用。
[实验探究]我们设计了如下装置,用制得的蓝绿色固体进行实验。

根据以上实验回答下列问题
(1)配制硫酸铜溶液的过程中滴加稀硫酸的作用是___________,所得硫酸铜溶液的溶质质量分数为_________
(2)实验室通常使用加热亚硝酸钠和氯化铵混合溶液的方法制取N2,该反应的化学方程为:__________。
⑶D装置加热前,需要首先打开活塞K,通入适量N2,然后关闭K,再点燃D处酒精灯。通入N2的作用___________, B为安全瓶,其作用原理为_________,C中盛装的试剂应是__________。
(4)加热D后观察到的现象是________________。
(5)经查阅文献知:Ksp[CaCO3]=2.8×10-9,Ksp[BaCO3]=5.1×10-9,经讨论认为需要用Ba(OH)2溶液代替澄清石灰水来定量测定蓝绿色固体的化学式,其原因是______________
a.Ba(OH)2的碱性比Ca(OH)2强
b.Ba(OH)2溶解度大于Ca(OH)2,能充分吸收CO2
c.相同条件下,CaCO3的溶解度明显大于BaCO3
d.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
(6)待D中反应完全后,打开活塞K,再次滴加NaNO2溶液产生N2,其目的是______________。若装置F中使用Ba(OH)2溶液,实验结束后经称量,装置E的质量增加0.27 g,F中产生沉淀1.97 g。则该蓝绿色固体的化学式为_____________。[写成xCuCO3·yCu(OH)2的形式]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 若把H2S分子写成H3S分子,违背了共价键的饱和性
B. H3O+的存在,说明共价键没有饱和性
C. 所有的共价键都有方向性
D. 凡是有空轨道的微粒,都能接受孤电子对形成牢固的配位键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com