
【题目】回答下列问题:
(1)下列反应中,属于放热反应的_________,属于吸热反应的是__________填序号)
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的炭 ⑤食物因氧化而腐败 ⑥Ba(OH)2·8H2O与NH4Cl反应 ⑦铁粉与稀盐酸反应
(2)断开1 mol H—H键、1 mol N—H键、1 mol N![]() N分别需要吸收能量为436 kJ、391 k、946kJ,则1 mol H2与足量N2反应生成NH3需__________(填“吸收”或“放出”)能量______kJ。(认为反应进行到底)。(小数点后保留两位数字)
N分别需要吸收能量为436 kJ、391 k、946kJ,则1 mol H2与足量N2反应生成NH3需__________(填“吸收”或“放出”)能量______kJ。(认为反应进行到底)。(小数点后保留两位数字)
(3)X、Y两种前20号主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,且X、Y两元素不在相邻的两个周期,则XY2的电子式为:____________。
【答案】①②③⑤⑦ ④⑥ 放出 30.67 ![]()
【解析】
(1)常见的放热反应有:物质燃烧、氧化反应、金属与酸反应、金属与水反应、中和反应、大多数化合反应和铝热反应;常见的吸热反应有:大多数分解反应,个别的化合反应(C和CO2)及某些复分解反应(如铵盐和强碱)。
(2)化学反应中,化学键断裂吸收能量,形成新的化学键放出能量,根据化学方程式计算吸收或放出的能量。
(3) 根据化学式判断元素化合价,由题中信息确定元素在元素同期表中的位置。
(1)①物质燃烧属于放热反应;②炸药爆炸属于放热反应;③酸碱中和反应属于放热反应;④二氧化碳通过炽热的炭属于化合反应,但为吸热反应;⑤食物因氧化而腐败属于放热反应;⑥Ba(OH)2·8H2O与NH4Cl反应属于吸热反应;⑦铁粉与稀盐酸反应属于吸热反应;所以属于放热反应的有:①②③⑤⑦,属于吸热反应的④⑥;
(2)在反应H2+![]() N2
N2![]() NH3中,按反应进行到底进行计算,断裂1 mol H—H键、
NH3中,按反应进行到底进行计算,断裂1 mol H—H键、![]() mol N
mol N![]() N键共吸收的能量为436 kJ+
N键共吸收的能量为436 kJ+![]() 946kJ=751.33 kJ,生成
946kJ=751.33 kJ,生成![]() mol NH3,放出能量为
mol NH3,放出能量为![]() 3391 kJ=782 kJ,吸收的能量少,放出的能量多,所以该反应为放热反应,放出的热量为782 kJ-751.33 kJ=30.67 kJ,答案为:放出;30.67;
3391 kJ=782 kJ,吸收的能量少,放出的能量多,所以该反应为放热反应,放出的热量为782 kJ-751.33 kJ=30.67 kJ,答案为:放出;30.67;
(3) X、Y两种前20号主族元素能形成XY2型离子化合物,则X为+2价,应该是第IIA族元素,Y为-1价,应该是第VIIA族元素,XY2中共有38个电子且不在相邻的两个周期,只能分别在第二、第四周期,X为Ca元素,为Y为F元素,CaF2为离子化合物,阴阳离子以离子键构成化合物,CaF2的电子式为![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】环氧树脂因其具有良好的机械性能、绝缘性能以及与各种材料的粘结性能,已广泛应用于涂料和胶黏剂等领域。下面是制备一种新型环氧树脂G的合成路线:


已知以下信息:

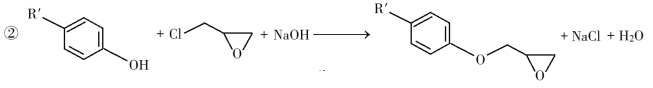
 回答下列问题:
回答下列问题:
(1)A是一种烯烃,化学名称为__________,C中官能团的名称为__________、__________。
(2)由B生成C的反应类型为__________。
(3)由C生成D的反应方程式为__________。
(4)E的结构简式为__________。
(5)E的二氯代物有多种同分异构体,请写出其中能同时满足以下条件的芳香化合物的结构简式__________、__________。
①能发生银镜反应;②核磁共振氢谱有三组峰,且峰面积比为3∶2∶1。
(6)假设化合物D、F和NaOH恰好完全反应生成1 mol单一聚合度的G,若生成的NaCl和H2O的总质量为765g,则G的n值理论上应等于__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对氨基苯甲酸酯类是一类局部麻醉药,化合物M是该类药物之一。合成M的一种路线如下:
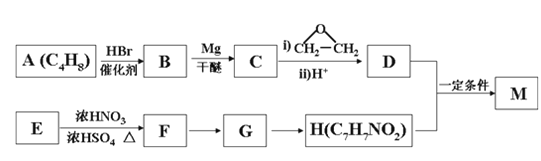
已知以下信息:①核磁共振氢谱显示B只有一种化学环境的氢,H苯环上有两种化学环境的氢。
②RX![]() RMgX
RMgX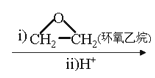 RCH2CH2OH。
RCH2CH2OH。
③E为芳香烃,其相对分子质量为92。
④![]() (苯胺,易被氧化)。
(苯胺,易被氧化)。
回答下列问题:
(1)A的结构简式为_________________,其化学名称是_____________________。
(2)由E生成F的化学方程式为_________________________________________。
(3)由G生成H的反应类型为__________________,H在一定条件下可以发生聚合反应,写出该聚合反应的化学方程式_______________________________________。
(4)M的结构简式为________________________________。
(5)D的同分异构体中不能与金属钠反应生成氢气的共有_____种(不考虑立体异构),其中核磁共振氢谱只有两组峰,且峰面积比为6:1的是_________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2FeO4在酸性或中性溶液中能快速产生O2,在碱性溶液中较稳定。如图是制备高铁酸钾的一种装置,制取实验完成后,取C中紫色溶液,加入稀盐酸,产生气体。下列说法不正确的是( )
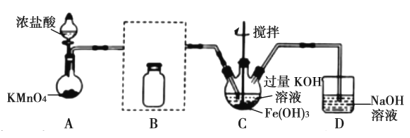
A.B瓶应盛放饱和食盐水除去混有的HCl
B.C瓶中KOH过量更有利于高铁酸钾的生成
C.加盐酸产生气体可说明氧化性:K2FeO4>Cl2
D.高铁酸钾是集氧化、吸附、絮凝等特点为一体的优良的水处理剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,用0.01molL-1NaOH溶液滴定10mL0.01molL-1H2A溶液的滴定曲线如图所示(已知:25℃时,H2A的Ka1=10-1.75,Ka2=10-7.19)。下列说法不正确的是( )
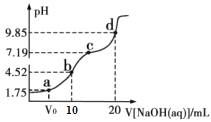
A.a点所得溶液中:V0=5mL
B.B点所得溶液中:c(H2A)+c(H+)= c(A2-)+c(OH-)
C.C点所得溶液中:c(Na+)>3 c(HA-)
D.D点所得溶液中A2-水解平衡常数Kh1=10-6.81
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按下图所示装置进行实验。

回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是__________________。
(2)以上装置中需要加热的仪器有_______ (填写字母),操作时应先点燃_____处的酒精灯。
(3)A装置中发生反应的化学方程式是____________________________。
(4)D装置的作用是____________________________。
(5)读取氮气的体积时,应注意①_________________;②_________________。
(6)实验中测得氮气的体积为VmL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有____________________。
A.生成二氧化碳气体的质量
B.生成水的质量
C.通人氧气的体积
D.氨基酸的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层的电子数之和。
(1)C2D电子式为__________,D原子的质子数和中子数相等,D的原子组成符号为______。
(2)用电子式表示A、B两元素形成AB2的过程_______________________________。
(3)E和A的最高价氧化物反应的化学方程式_________________________________。
(4)足量的AB2与C的最高价氧化物对应水化物反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)按系统命名法填写下列有机物的名称:
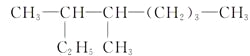 的名称是____________________。
的名称是____________________。
(2)2,6-二甲基-4-乙基辛烷的结构简式是______________,1 mol该烃完全燃烧需消耗氧气________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法不正确的是( )

A. 该晶体属于离子晶体
B. 晶体的化学式为Ba2O2
C. 该晶体晶胞结构与NaCl相似
D. 与每个Ba2+距离相等且最近的Ba2+共有12个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com