
【题目】如图是恒温下某反应的化学反应速率随反应时间变化的示意图.下列叙述与示意图不相符合的是( ) 
A.反应达平衡时,正反应速率和逆反应速率相等
B.该反应达到平衡状态Ⅰ后,减小反应物浓度,平衡发生移动,达到平衡状态Ⅱ
C.该反应达到平衡状态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡状态Ⅱ
D.同一种反应物在平衡状态Ⅰ和平衡状态Ⅱ时浓度不相等
【答案】B
【解析】解:A.正逆反应速率相等,可逆反应达到平衡状态,为动态平衡状态,故A不选;
B.可逆反应中物质浓度与反应速率成正比,该反应达到平衡状态Ⅰ后,减小反应物浓度瞬间,正反应速率减小、逆反应速率不变,平衡发生移动,所以图象不符合,故B选;
C.增大反应物浓度瞬间,正反应速率增大、逆反应速率不变,平衡向正反应方向移动,从而达到新的平衡状态,新的平衡状态中浓度大于原来平衡状态,所以反应速率大于原来平衡状态,图象符合,故C不选;
D.物质浓度越大反应速率越大,根据图知,II状态反应速率大于I状态,所以II状态浓度大于I状态,符合图象,故D不选;
故选B.
可逆反应达到平衡状态时,正逆反应速率相等,为动态平衡状态;可逆反应中物质浓度与反应速率成正比,所以温度浓度越大,反应速率越大.


 小学教材全测系列答案
小学教材全测系列答案科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是( )
A.σ键比π键的重叠程度大,形成的共价键强度大
B.两个原子之间形成共价键时,最多有一个σ键
C.气体单质中,一定有σ键,可能有π键
D.N2分子中有一个σ键、2个π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=﹣Q1 kJmol﹣1
2H2(g)+O2(g)═2H2O(g);△=﹣Q2 kJmol﹣1 ,
2H2(g)+O2(g)═2H2O(l);△H2=﹣Q3 kJmol﹣1
常温下,取体积比2:3的甲烷和氢气的混合气体11.2L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为( )
A.0.4Q1+0.15Q2
B.0.2Q1+0.05Q2
C.0.2Q1+0.15Q3
D.0.2Q1+0.3Q2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( ) 
A.常压下五种元素的单质中,Z单质的沸点最高
B.Y、Z的阴离子电子层结构都与R原子的相同
C.Y的氢化物的沸点比H2O的沸点高
D.Y元素的非金属性比W元素的非金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 镍氢电池、锂电池和碱性锌锰干电池都是二次电池
B. 氢氧燃料电池是一种高效且不会污染环境的新型电池
C. 铅蓄电池放电的时候正极材料是铅,负极材料是二氧化铅
D. 铅蓄电池充电时将化学能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、人类生产、社会可持续发展密切相关,下列说法正确的是
A.合成材料、光伏材料和复合材料都是新型无机非金属材料
B.大米、.玉米、小麦中的淀粉经水解可变成乙醇
C.利用二氧化碳制造全降解塑料,可以减少白色污染
D.煤的干馏是化学变化,煤的气化、液化和石油的分馏都是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着我国汽车年销量的大幅增加,空气环境受到了很大的污染.汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )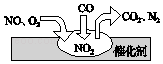
A.反应中NO为氧化剂,N2为氧化产物
B.汽车尾气的主要污染成分包括CO、NO和N2
C.NO和O2必须在催化剂表面才能反应
D.催化转化总化学方程式为2NO+O2+4CO=4CO2+N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程: 
(1)固体I中主要成分为 , 捕获剂所捕获的气体主要是 .
(2)处理含NH4+废水时,发生反应的离子方程式为 .
(3)若X为适量空气,严格控制空气用量的原因是 .
(4)工业废气中的SO2、NO还可采用NaClO2溶液作为吸收剂进行净化,在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为5×10﹣3molL﹣1 . 反应一段时间后溶液中离子浓度的分析结果如表:
离子 | SO42﹣ | SO32﹣ | NO3﹣ | NO2﹣ | Cl﹣ |
c(molL﹣1) | 8.35×10﹣4 | 6.87×10﹣6 | 1.5×10﹣4 | 1.2×10﹣5 | 3.4×10﹣3 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式 .
增加压强,NO的转化率(填“提高”、“不变”或“降低”).
②随着吸收反应的进行,吸收剂溶液的pH逐渐(填“增大”、“不变”或“减小”).
③如果采用NaClO、Ca(ClO)2替代NaClO2 , 也能得到较好的烟气脱硫效果.从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com