
在室温下,100ml 0.1mol/L的醋酸溶液中,欲使其溶液的pH值减小,但又要使醋酸电离程度减少,应采取( )
A.加入少量CH3COONa固体 B.通入少量氯化氢气体
C.提高温度 D.加入少量纯醋酸
科目:高中化学 来源:2012-2013学年甘肃省武威第五中学高二11月月考化学试卷(带解析) 题型:单选题
在室温下,100ml 0.1mol/L的醋酸溶液中,欲使其溶液的pH值减小,但又要使醋酸电离程度减少,应采取( )
| A.加入少量CH3COONa固体 | B.通入少量氯化氢气体 |
| C.提高温度 | D.加入少量纯醋酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:
为测定碘酸铜[Cu(IO3)2]的溶解度,在室温下取100mL碘酸铜饱和溶液,加入过量酸化的KI溶液。充分反应后,再用0.130mol?L-1Na2S2O3溶液滴定生成的碘,消耗Na2S2O3溶液35.0mL。反应过程如下: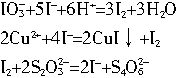
(1)实验中参加反应的Cu(IO3)2的物质的量是____mmol。
(2)碘酸铜在室温下的溶解度为____g?L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
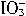 +5I-+6H+=3I2+3H2O
+5I-+6H+=3I2+3H2O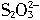 =2I-+
=2I-+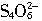
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com