
| A、该合金的熔点介于钠、铝之间 |
| B、钠或铝形成的氧化物均为碱性氧化物 |
| C、钠和铝分别与不足量的盐酸反应,所得溶液均呈中性 |
| D、若合金中n(Na)>n(Al),将其投入到足量的水中,可得无色透明溶液 |


科目:高中化学 来源: 题型:
| A、既能溶解Al(OH)3,又能溶解H2SiO3的溶液:Na+、Fe2+、SO42-、Cl- |
| B、强碱性溶液中:Cl-、SO32-、HSO3-、Na+ |
| C、c(HCO3-)=0.1mol/L的溶液中:Na+、K+、CO32-、Br- |
| D、含有大量Fe3+的溶液:Na+、Al3+、NO3-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:
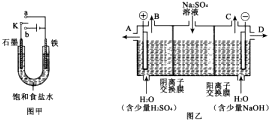 (1)某课外活动小组同学用图甲装置进行实验,试答下列问题:
(1)某课外活动小组同学用图甲装置进行实验,试答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、放在足量水中 |
| B、放在足量盐酸中 |
| C、放在足量CuSO4溶液中 |
| D、用刺有小孔的铝,包好放入足量水底中(假设铝不参加反应) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2、HClO |
| B、Cl、Cl-、Cl2 |
| C、Cl2、Cl-、H+、ClO-、H2O和极少量OH- |
| D、Cl2、Cl-、H+、HClO、ClO-、H2O和极少量OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该化合物是共价化合物 |
| B、化合物N5AsF6中As化合价为+1 |
| C、N5+共有34个核外电子 |
| D、N5+中氮-氮原子间以共用电子对结合 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、②③④ |
| C、①②④ | D、①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A-B | A=B | A≡B | |
| C≡O | 357.7 | 798.9 | 1071.9 |
| N≡N | 154.8 | 418.4 | 941.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com