
| A、硝酸银溶液与氯化钠溶液混合:Ag++Cl-=AgCl↓ |
| B、铁跟稀硫酸反应:Fe+2H+=Fe2++H2↑ |
| C、碳酸钙与稀盐酸反应:CO32-+2H+=H2O+CO2↑ |
| D、氧化铜与稀盐酸反应:CuO+2H+=Cu2++H2O |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、赤潮是水体富营养化结果 |
| B、含磷洗衣粉广泛使用与排放是发生赤潮的原因之一 |
| C、封闭的海湾更易发生 |
| D、赤潮的发生是与人类活动无关的自然现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、13g乙炔和苯的混合液中总原子数为2NA |
| B、4℃时9mL水和11.2L氮气含有相同的分子数 |
| C、同温同压下,NA个NO2与NA个N2和O2的混合气体的体积不相等 |
| D、1.01×105Pa时,11.2 L氧气所含的原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用Fe2(SO4)3净水 |
| B、用高纯度的SiO2制造光电池 |
| C、用Na2SiO3制备木材防火剂 |
| D、用Na2O2作呼吸面具中氧气的来源 |
查看答案和解析>>
科目:高中化学 来源: 题型:

A、C+CO2
| ||||
| B、Zn+H2SO4=ZnSO4+H2↑ | ||||
C、CH4+2O2
| ||||
| D、KOH+HNO3=KNO3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、28 g N2中含有氮原子数为NA |
| B、1 mol Na与足量O2反应转移的电子数为NA |
| C、常温常压下,22.4LCO2中含有的分子数为NA |
| D、1 mol?L-1K2SO4溶液中含有的钾离子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
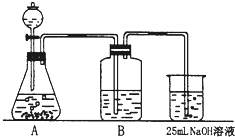 Na2CO3是一种很重要的化学物质,某学生拟在实验室中制备.下面是他的实验过程.用50mL NaOH溶液吸收CO2气体制备Na2CO3.为了防止通入的CO2过量而生成NaHCO3,他设计了如下步骤:
Na2CO3是一种很重要的化学物质,某学生拟在实验室中制备.下面是他的实验过程.用50mL NaOH溶液吸收CO2气体制备Na2CO3.为了防止通入的CO2过量而生成NaHCO3,他设计了如下步骤:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com