
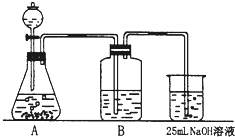
 Na2CO3��һ�ֺ���Ҫ�Ļ�ѧ���ʣ�ijѧ������ʵ�������Ʊ�������������ʵ����̣���50mL NaOH��Һ����CO2�����Ʊ�Na2CO3��Ϊ�˷�ֹͨ���CO2����������NaHCO3������������²��裺
Na2CO3��һ�ֺ���Ҫ�Ļ�ѧ���ʣ�ijѧ������ʵ�������Ʊ�������������ʵ����̣���50mL NaOH��Һ����CO2�����Ʊ�Na2CO3��Ϊ�˷�ֹͨ���CO2����������NaHCO3������������²��裺

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������Һ���Ȼ�����Һ��ϣ�Ag++Cl-=AgCl�� |
| B������ϡ���ᷴӦ��Fe+2H+=Fe2++H2�� |
| C��̼�����ϡ���ᷴӦ��CO32-+2H+=H2O+CO2�� |
| D������ͭ��ϡ���ᷴӦ��CuO+2H+=Cu2++H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ʹ�ô�����Ϊ������ѧ��Ӧ���� |
| B������������Ũ�ȿ�����Ӧ���� |
| C�������������£�������ȫ��ת��Ϊ���� |
| D���ﵽƽ��ʱ����ϵ�и����ʵ�Ũ�Ȳ��ٸı� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| t/min | CO/mol | H2/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.10 |
| 3 | 0.75 | 0.50 | 0.25 |
| 5 | 0.65 | 0.30 | 0.35 |
| 7 | 0.55 | 0.10 | 0.45 |
| 9 | 0.55 | 0.10 | 0.45 |
| 10 | 0.55 | 0.10 | 0.45 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���ϱ� | ���ƺ��Ρ������ |
| ������ | 20kg/kg��40mg/kf |
| ����ŷ� | �ܷ⡢�ܹ⡢���� |
| ʳ�÷��� | ���ʱ����ʳƷ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��HCO3-+H2O�TH2CO3+OH- |
| B��CO32-+2H2O�TH2CO3+2OH- |
| C��Fe3++3H2O?Fe��OH��3+3H+ |
| D��NH4++H2O?NH3?H2O+OH- |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com