
| A、1mol Na加热时与O2反应失去的电子数目为NA |
| B、92g N2O4和92g NO2含有的原子数均为6NA |
| C、1L 0.1mol?L-1的盐酸中,所含HCl分子数为0.1NA |
| D、标准状况下,22.4L O3中含3NA个氧原子 |


 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
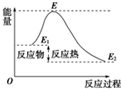
| A、反应物分子(或离子)间的每次碰撞是反应的先决条件 |
| B、反应物的分子的每次碰撞都能发生化学反应 |
| C、活化分子具有比普通分子更高的能量,催化剂能够减低活化能的数值 |
| D、活化能是活化分子的平均能量与所有分子平均能量之差,如图所示正反应的活化能为E-E1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有NA个氦原子的氦气在标准状况下的体积约为11.2 L |
| B、25℃,1.01×105 Pa,64 g SO2中含有的原子数为3NA |
| C、在常温常压下,11.2 L Cl2含有的分子数为0.5 NA |
| D、标准状况下,11.2 L H2O含有的分子数为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
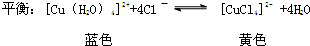
查看答案和解析>>
科目:高中化学 来源: 题型:
 铜和镍是第四周期重要的过渡元素,它们的单质及化合物具有广泛用途,请回答以下问题:
铜和镍是第四周期重要的过渡元素,它们的单质及化合物具有广泛用途,请回答以下问题: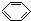 ④HCHO,其中碳原子采取sp2杂化的分子有
④HCHO,其中碳原子采取sp2杂化的分子有查看答案和解析>>
科目:高中化学 来源: 题型:
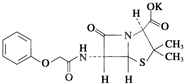 下列有关说法错误的是( )
下列有关说法错误的是( )| A、青霉素V钾为芳香族化合物 |
| B、青霉素V钾的分子式为C16H17KN2O5 |
| C、青霉素V钾在酸性条件下最终生成青霉氨基酸 |
| D、使用本品前需先进行青霉素皮肤敏感试验 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com