
已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| 温度/°C | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K=________,ΔH________0(填“<”“>”“=”);
(2)830°C时,向一个5 L的密闭容器中充入0.20 mol的A和0.80 mol的B,如反应初始6 s内A的平均反应速率v(A)=0.003 mol·L-1·s-1,则6 s时C的物质的量为______mol;若反应经一段时间后,达到平衡时A的转化率为________,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为________;
(3)判断该反应是否达到平衡的依据为________(填正确选项前的字母);
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时间改变 d.单位时间里生成C和D的物质的量相等
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
关于钠的叙述中,正确的是 ( )
A.钠是银白色金属,硬度很大
B.将金属钠放在石棉网上用酒精灯加热,熔化后剧烈燃烧,产生黄色火焰,生成淡黄色固体
C.金属钠在空气中燃烧,生成氧化钠
D.金属钠的熔点很高
查看答案和解析>>
科目:高中化学 来源: 题型:
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、Al3+和五种阴离子Cl-、OH-、NO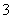 、CO
、CO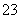 、X中的一种。
、X中的一种。
(1) 某同学通过比较分析认为无须检验就可判断其中必有的两种物质是_______ 和_________。
(2) 物质C中含有离子X。为了确定X,现将(1)中的两种物质记为A和B,当C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体,则X为________(填字母)。
A.Br- B.SO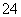 C.CH3COO- D.HCO
C.CH3COO- D.HCO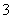
(3) 将19.2 g Cu投入装有足量D溶液的试管中,Cu不溶解,再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,写出Cu溶解的离子方程式 ,若要将Cu完全溶解,至少加入H2SO4的物质的量是____________________。
(4) E溶液与氢碘酸反应时可生成棕色物质,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
反应P(g)+Q(g)⇌M(g)+N(s)△H<0,达到平衡时,下列说法正确的是( )
|
| A. | 减小容器体积,平衡不移动 | B. | 加入催化剂,M的产率增大 |
|
| C. | 增大c(P),P的转化率增大 | D. | 降低温度,Q的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
对于在一密闭容器中进行的下列反应:C(s)+ O2(g) CO2(g)下列说法中错误的是
CO2(g)下列说法中错误的是
A.将木炭粉碎成粉末状可以加快化学反应速率
B.升高温度可以加快化学反应速率
C.增加压强不能加快化学反应速率
D.增加木炭的量可以加快化学反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于“化学与健康”的说法不正确的是
A.“血液透析”利用了胶体的性质 B.服用铬含量超标的药用胶囊会对人对健康造成危害
C.光化学烟雾不会引起呼吸道疾病 D.食用一定量的油脂能促进人体对某些维生素的吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
以NA表示阿伏伽德罗常数,下列说法中正确的是
A.58.5g氯化钠固体中含有NA个氯化钠分子
B.5.6 g铁粉与酸反应失去的电子数一定为0.2NA
C.6.0g金刚石中含有的共价键数为NA
D.标况下,11.2LSO3所含的分子数为0.5NA
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W四种常见元素,其中X、Y、Z为短周期元素。已知:① X的最高价氧化物对应的水化物为无机酸中最强酸,ZX4分子是由粗Z提纯Z的中间产物 ②Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料 ③ Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料 ④W的常见化合价有+3、+2,WX3稀溶液呈黄色。
(1)W(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为 。
(2)X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为 。
(3)Z的氧化物在通讯领域用来作 ,工业上制Z单质的化学反应方程式为 。
(4)在50mLlmol·L-1的YX3溶液中逐滴加入0.5mol·L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积最多为 mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
锌锰干电池由于其贮存和使用寿命较短,大都为一次性电池,用完之后被当作垃圾扔掉。这不仅浪费了宝贵的金属资源,而且还会产生严重的环境污染。下表是各类电池的综合成分分析结果:
| 元素 | 锌 | 锰 | 铁 | 铜 | 碳 | 其它 |
| 质量百分含量 | 13~27 | 14~28 | 23~26 | 0.5~0.7 | 5~6 | 13 |
通过简单的机械处理,将电池中各组分进行最大在限度的分离,从而使整个处理过程得到简化。再分别对锌皮和锰粉(MnO2)进行湿法处理,通过预处理、浸取、净化等工序制出产品。工艺流程如下图:
查阅资料知各离子沉淀完全的pH为
| 离子 | Fe3+ | Fe2+ | Cu2+ | Mn2+ |
| pH | 3.2 | 9.0 | 6.7 | 10.1 |
已知:锌元素与铝元素相似,具有两性。
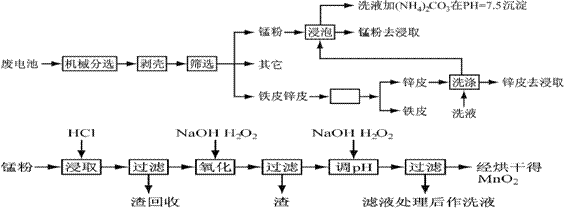
1、市售锌锰干电池为碱性电池,电解质溶液为KOH,则其正极反应为 ;
电极总反应方程为 ;
2、在预处理中,分离铁皮和锌皮的方法是 ,洗液加(NH4)2CO3在pH=7.5沉淀出一种碱式盐,该物质的化学式为 。
3、二氧化锰生产中,写出加入30%盐酸溶解时的离子方程式 ;盐酸溶解后回收的渣是 ;
4、已知第二次加H2O2后调节pH≈9的目的为将Mn2+转化为MnO2,则第一次加H2O2后调节pH≈5,目的是 ;
5、实验室中用高锰酸钾溶液检验Mn2+时,产生黑色沉淀,该反应的离子方程式为
;
硫酸锰在高温条件下可以得到三种氧化物,该热分解的方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com