
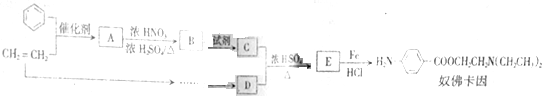
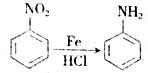
 ,生成A的反应类型为加成反应.
,生成A的反应类型为加成反应.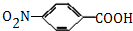 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O. 等.
等.分析 根据题中信息及奴佛卡因的结构可推知,E为 ,结合各物质转化关系,苯与乙烯反应生成A的生产工艺的原子利用率为100%,则该反应为苯与乙烯发生加成反应生成A为
,结合各物质转化关系,苯与乙烯反应生成A的生产工艺的原子利用率为100%,则该反应为苯与乙烯发生加成反应生成A为 ,A在浓硫酸的作用下发生硝化反应得B为
,A在浓硫酸的作用下发生硝化反应得B为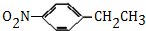 ,B发生氧化反应得C为
,B发生氧化反应得C为 ,结合C和E的结构可知,C与D发生酯化反应生成E,所以D为HOCH2CH2N(CH2CH3)2,据此答题;
,结合C和E的结构可知,C与D发生酯化反应生成E,所以D为HOCH2CH2N(CH2CH3)2,据此答题;
解答 解:根据题中信息及奴佛卡因的结构可推知,E为 ,结合各物质转化关系,苯与乙烯反应生成A的生产工艺的原子利用率为100%,则该反应为苯与乙烯发生加成反应生成A为
,结合各物质转化关系,苯与乙烯反应生成A的生产工艺的原子利用率为100%,则该反应为苯与乙烯发生加成反应生成A为 ,A在浓硫酸的作用下发生硝化反应得B为
,A在浓硫酸的作用下发生硝化反应得B为 ,B发生氧化反应得C为
,B发生氧化反应得C为 ,结合C和E的结构可知,C与D发生酯化反应生成E,所以D为HOCH2CH2N(CH2CH3)2,
,结合C和E的结构可知,C与D发生酯化反应生成E,所以D为HOCH2CH2N(CH2CH3)2,
(1)根据奴佛卡因的结构简式可知其分子式为C13H20N2O2,其含氧官能团的名称是酯基,
故答案为:C13H20N2O2;酯基;
(2)苯与乙烯反应生成A的生产工艺的原子利用率为100%,则A的结构简式为 ,生成A的反应类型为加成反应,
,生成A的反应类型为加成反应,
故答案为: ;加成反应;
;加成反应;
(3)C+D→E反应的化学方程式为HOCH2CH2N(CH2CH3)2+ $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O,
+H2O,
故答案为:HOCH2CH2N(CH2CH3)2+ $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O;
+H2O;
(4)B为 ,同时符合下列条件a.分子中含有羧基和苯环;b.苯环上有两种不同化学环境的氢原子,说明有两个处于对位的基团,则符合条件的B的一种同分异构体的结构简式为
,同时符合下列条件a.分子中含有羧基和苯环;b.苯环上有两种不同化学环境的氢原子,说明有两个处于对位的基团,则符合条件的B的一种同分异构体的结构简式为 等,
等,
故答案为: 等.
等.
点评 本题考查有机物的合成及推断,题目难度较大,注意在有机合成中渗透了苯环取代中的邻对位基团和间位基团的选择,同时考查了同分异构体的书写,利用好流程图中信息.


科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③④⑤ | C. | ①④⑤ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
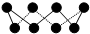
| A. | ①②③④⑤ | B. | ①③④⑤⑥ | C. | ②③⑤⑥ | D. | ③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
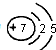 ;
; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
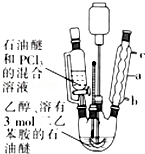 亚磷酸三乙酯[P(OC2H5)3]常用作塑料稳定剂、增塑剂,也用作医药、农药的中间体.其合成原理为PCl3+3C2H5OH$\stackrel{△}{→}$P(OC2H5)3+3HCl
亚磷酸三乙酯[P(OC2H5)3]常用作塑料稳定剂、增塑剂,也用作医药、农药的中间体.其合成原理为PCl3+3C2H5OH$\stackrel{△}{→}$P(OC2H5)3+3HCl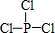 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
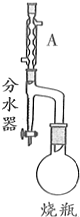 实验室制备甲基丙烯酸甲酯的反应装置示意图和有关信息如下:
实验室制备甲基丙烯酸甲酯的反应装置示意图和有关信息如下:
| 药品 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度(g•cm-3) |
| 甲醇 | 32 | -98 | -64.5 | 与水混溶,易溶于有机溶剂 | 0.79 |
| 甲基丙烯酸 | 86 | 15 | 161 | 溶于热水,易溶于有机剂 | 1.01 |
| 甲基丙烯酸甲酯 | 100 | -48 | 100 | 微溶于水,易溶于有机溶剂 | 0.944 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时,应使温度计水银球与蒸馏烧瓶支管口在同一高度处 | |
| C. | 在苯甲酸重结晶实验中,粗苯甲酸加热溶解后,还需加少量蒸馏水再趁热过滤 | |
| D. | 除去混在苯中的苯酚时,可先加入饱和浓溴水,振荡后静置,再过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2晶体易溶于水,水溶液呈现酸性 | |
| B. | CO2通入水玻璃中不可能得到硅酸 | |
| C. | SiO2是酸性氧化物,它不溶于任何酸 | |
| D. | SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑是制造玻璃的反应之一 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com