
设NA表示阿伏加德罗常数的值,下列说法正确的是
A.5.6 g Fe和足量的盐酸完全反应失去电子数为0.3 NA
B.22.4L SO2含有NA个SO2分子
C.1.6g CH4所含的电子数为NA
D.标况下,4.48L的水中含有H2O分子的数目为0.2NA
科目:高中化学 来源: 题型:
把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为 ( )
A.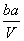 mol·L-1 B.
mol·L-1 B.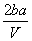 mol·L-1C.
mol·L-1C. 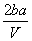 mol·L-1 D.
mol·L-1 D.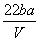 mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是某种常见金属的部分性质:
| 颜色状态 | 硬度 | 密度 | 熔点 | 导电性 | 导热性 | 延展性 |
| 银白色固体 | 较软 | 2.70 g·cm-3 | 660.4℃ | 良好 | 良好 | 良好 |
将该金属投入冷水中无变化,投入稀盐酸中可产生大量的无色气体。试回答:
(1)推断该金属可能的一种用途:________,该金属的活泼性比铜________(填“强”或“弱”)。
(2)请自选试剂,设计不同的实验方案探究该金属与铁的活泼性强弱,并完成下表:
| 猜想 | 验证方法 | 预测实验现象 |
| 该金属比铁活泼 | ||
| 该金属活泼性比铁弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组设计如下微型实验装置。实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发 现电流表指针偏转,下列有关描述正确的是
现电流表指针偏转,下列有关描述正确的是

A.断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl-  Cl2↑+H2↑
Cl2↑+H2↑
B.断开K2,闭合K1时,石墨电极附近溶液变红
C.断开K1,闭合K2时,石墨电极作正极
D.断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e-=== 2Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。
(1)电解饱和食盐水的化学方程 式为 ▲ 。
式为 ▲ 。
 (2)常温下,某化学兴趣小组在实验室中,用石墨电极以右图装置进行电解某浓度氯化钠溶液的实验,电解一段时间后,收集到标准状况下氢气2.24L。(设电解前后溶液的体积均为1 L,不考虑水的消耗或气体的溶解)
(2)常温下,某化学兴趣小组在实验室中,用石墨电极以右图装置进行电解某浓度氯化钠溶液的实验,电解一段时间后,收集到标准状况下氢气2.24L。(设电解前后溶液的体积均为1 L,不考虑水的消耗或气体的溶解)
①理论上,电解后溶液中c(OH—)= ▲ mol/L。
②若实际测得反应后溶液的c(OH—)=0.1mol/L,则造成这种误差的原因可能是:
a.2H2O 2H2↑+O2↑;若仅考虑该原因,则电解过程中溶液减小的质量是 ▲ g。
2H2↑+O2↑;若仅考虑该原因,则电解过程中溶液减小的质量是 ▲ g。
b.还可能为 ▲ (用离子方程式表示)。
③经测定,该实验中溶液实际减少的质量为4.23g,则所产生的气体及其物质的量之比为
▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对有关实验事实的解释正确的是
A.向某溶液中滴加氯水后,再加入KSCN溶液,溶液呈红色,说明原溶液中含有Fe2+
B.浓硫酸和浓盐酸长期暴露在空气中浓度均降低,原理不相同
C.向某溶液中加入氯化钡溶液,生成白色沉淀,再加入稀盐酸,沉淀不溶解,则原溶液一定含有SO42
D.常温下,浓硫酸可以用铁质容器储运,说明铁与冷的浓硫酸不反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.金属在反应中只能作还原剂,非金属在反应中只能作氧化剂
B.氧化剂在反应中失去电子,还原剂在反应中得到电子
C.氧化剂具有氧化性,还原剂具有还原性
D.阳离子只有氧化性,阴离子只有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1.505×1023个X气体分子的质量为8 g,则X气体的摩尔质量是( )
A.16 g B.32 g
C.64 g/mol D.32 g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的性质,不是由于氢键引起的是
A.沸点:H2O>H2S B.溶解性:NH3(易溶于水)>PH3(难溶于水)
C.稳定性:H2O>H2S D.等质量时体积: 冰>水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com