
反应2A(g)⇌2B(g)+E(g)△H>0,达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是( )
|
| A. | 加压 | B. | 减压 | C. | 减小E的浓度 | D. | 降温 |
| 化学平衡的影响因素;化学反应速率的影响因素.. | |
| 专题: | 化学平衡专题. |
| 分析: | 达平衡时,要使v正降低,可采取降低温度、减小压强或减小浓度的措施,使c(A)增大,应使平衡向逆反应方向移动,据此结合外界条件对平衡移动影响分析. |
| 解答: | 解:A.增大压强,平衡向逆反应方向移动,A的浓度增大,正、逆反应速率都增大,故A错误; B.降低压强,正、逆速率都减小,平衡向正反应方向移动,A的浓度降低,故B错误; C.减少E的浓度,平衡向正反应方向移动,正、逆速率都减小,但A的浓度降低,故C错误; D.降低温度,正、逆反应速率都减小,平衡向逆反应方向移动,A的浓度增大,故D正确. 故选B. |
| 点评: | 本题考查外界条件对化学平衡的影响,难度不大,本题注意根据反应方程式的特征判断平衡移动的方向. |


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
在某无色透明的酸性溶液中,能大量存在的离子组是 ( )
A.Na+ 、K+、SO42-、HCO3- B.Cu2+、K+、SO42-、NO3-
C.Na+、 K+、Cl-、 NO3- D.Fe3+、K+、SO42-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
已知测定中和热的实验步骤如下:①量取50mL 0.25 mol/L硫酸倒入小烧杯中,测量温度; ②量取50mL 0.55mol/L NaOH溶液,测量温度; ③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度。请回答:
(1)NaOH溶液稍过量的原因 。
(2)加入NaOH溶液的正确操作是 (填字母)。
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(3)使硫酸与NaOH溶液混合均匀的正确操作是 。
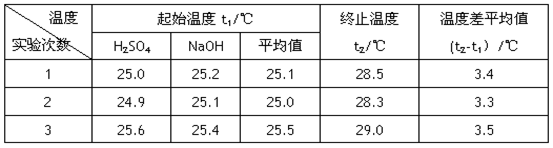
(4)设溶液的密度均为1g·cm-3,中和后溶液的比热c=4.18J·(g·℃)-1,请根据实验数据求出中和热为 ,写出该反应的热化学方程式_________
(5)若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量 (填“小于”、“等于”或“大于”)57.3 kJ,
查看答案和解析>>
科目:高中化学 来源: 题型:
某混合气体由一氧化碳和二氧化碳组成,若混合气体在标准状况下的密度是1.875g/L,则混合气体中一氧化碳和二氧化碳的体积比是:( )
A.1:3 B.3:1 C.1:7 D.7:1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列既属于氧化还原反应,又属于吸热反应的是( )
A.铝片与稀盐酸反应 B.Ba(OH)2•8H2O与NH4Cl的反应
C.灼热的炭与水蒸气的反应 D.甲烷(CH4)在O2中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
将2.0mol SO2气体和2.0mol SO3气体混合于固定体积的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)⇌2SO3(g),达到平衡时SO3为n mol.在相同温度下,分别按下列配比在相同密闭容器中放入起始物质,平衡时SO3等于n mol的是( )
|
| A. | 1.6 mol SO2+0.3 mol O2+0.4 mol SO3 |
|
| B. | 4.0 mol SO2+2.0 mol O2 |
|
| C. | 2.0 mol SO2+1.0 mol O2+2.0 mol SO3 |
|
| D. | 3.0 mol SO2+0.5 mol O2+1.0 mol SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知化学反应①Fe(s)+CO2(g)⇌FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)⇌FeO(s)+H2(g),其平衡常数为K2.在温度973K 和1173K 情况下,K1、K2的值分别如下:
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
(1)通过表格中的数值可以推断:反应①是 吸热 (填“吸热”或“放热”)反应.
(2)现有反应③:CO2(g)+H2(g)⇌CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3= 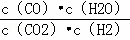 .
.
(3)能判断反应③已达平衡状态的是 BC .
A.容器中压强不变 B.混合气体中c(CO)不变 C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(4)根据反应①与②可推导出K1、K2与K3之间的关系式 K3=K1•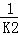 .据此关系式及上表数据,也能推断出反应③是 吸热 (填“吸热”或“放热”)反应.要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施是 DF (填写序号).
.据此关系式及上表数据,也能推断出反应③是 吸热 (填“吸热”或“放热”)反应.要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施是 DF (填写序号).
A.缩小反应容器容积 B.扩大反应容器容积 C.降低温度 D.升高温度 E.使用合适的催化剂 F.设法减少CO的量.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学实验操作或事故处理方法不正确的是 ( )
A.碱沾到皮肤上时,应立即用大量水冲洗,再涂上硼酸溶液
B.浓硫酸沾到皮肤上时,可立即用大量水冲洗,然后涂上3%~5%的NaHCO3溶液
C.酒精灯不慎碰倒起火时,可用湿抹布或沙子盖灭,不能用水泼灭
D.配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
关于铷的结构、性质和保存的判断,错误的是( )
①原子半径比对应离子半径大;②与水剧烈反应,浮在水面上;③比钾活泼,极易被还原;④它的氧化物能跟二氧化碳反应 ⑤可保存在煤油中
A.①② B.②③ C.③④ D.④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com