
| A、C(s)+O2(g)=CO2(g);△H=-315kJ |
| B、NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.3kJ?mol-1 |
| C、C2H5OH+3O2=2CO2+3H2O;△H=-1368.8kJ?mol-1 |
| D、2H2O(g)=2H2(g)+O2(g);△H=-483.6kJ?mol-1 |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
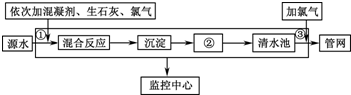 如图是目前我国城市饮用水的生产流程,生活饮用水水质的标准主要有:色度、浑浊度、pH、细菌总数、气味等.
如图是目前我国城市饮用水的生产流程,生活饮用水水质的标准主要有:色度、浑浊度、pH、细菌总数、气味等.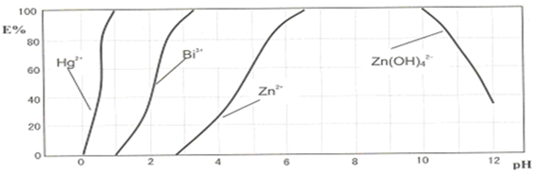
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、上述反应中氧化剂和还原剂的物质的量之比为5:6 |
| B、产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾) |
| C、上述反应中消耗3 mol P时,转移电子的物质的量为10mol |
| D、上述火药中的红磷可以用白磷代替 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 研究确定六氟化硫分子为正八面体构型(分子结构如图所示),难溶于水,在高温下仍有良好的绝缘性,在电器工业方面具有广泛用途.下列推测正确的是( )
研究确定六氟化硫分子为正八面体构型(分子结构如图所示),难溶于水,在高温下仍有良好的绝缘性,在电器工业方面具有广泛用途.下列推测正确的是( )| A、SF6中各原子均达到8电子稳定结构 |
| B、SF6分子中既含有非极性共价键键又含有极性共价键 |
| C、SF6分子是含有极性键的非极性分子 |
| D、SF6可能是原子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、晶体硅熔点高硬度大,可用于制作半导体材料 |
| B、浓硫酸具有酸性,可用于刻蚀玻璃制品 |
| C、漂白粉在空气中不稳定,可用于漂白纸张 |
| D、氢氧化铝具有弱碱性,可用于制胃酸中和剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ?mol-1 | 436 | 391 | 945 |
| 5 |
| 4 |
| 1 |
| 4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com