
【题目】铝及其化合物广泛应用于金属冶炼和有机合成等领域。
(1)铝热反应可以冶炼金属铬,基态铬原子的核外电子排布式为:_______________________。
(2)AlCl3可用作下列反应的催化剂

①乙酸酐分子中发生sp3杂化的原子共有______个
②CH3COOH和H2O可以以任意比例互溶,其原因是它们均是极性分子和_________________。
③单个AlCl3分子的空间构型为_______。
(3)在氧化铝的作用下,N4H4(SO4)2可同碱反应生成一种类似白磷的N4分子,1molN4分子中含有的共价键的物质的量为_____mol
(4)某遮光剂的晶胞如图甲(黑球为Na+,白球为AlFn(n-3)-阴离子),由图可推算知,n=________。

(5)由Fe和Y形成的某化合物的晶胞如图乙所示,该晶胞中与亚铁离子距离相等并且最近的亚铁离子有_____个。 另有一种有缺陷的Fe和Y形成的化合物的晶体由Fe2+,Fe3+,Y2-及空隙组成,可表示为Fe0.98Y,则该晶体中,n(Fe2+) : n(Fe3+) =______________。
【答案】 1s22s22p63s23p63d54s1或者[Ar]3d54s1 3 乙酸与水分子间能形成氢键 平面三角形 6 6 12 47:2
【解析】(1)1s22s22p63s23p63d54s1或者[Ar]3d54s1
(2)①从乙酸酐的分子结构上可以看出来,乙酸酐中VSEPR模型为正四面体型的C原子有2个O原子有1个,所以采取sp3杂化的原子共有3个。
②乙酸与水分子间能形成氢键。
③AlCl3属于共价化合物,中心原子为Al原子,Al原子最外层共3个电子,形成了3个σ键,没有孤电子对,VSEPR模型为平面三角形,实际构型为平面三角形。
(3)白磷的结构为正四面体结构,一个白磷分子中有6个共价键,所以1mol N4分子中包含的共价键为6mol。
(4)晶胞中包含的Na+数量为10×1/2+4×1/4=6,AlFn(n-3)-的数量为1+8×1/8=2,分子式为Na3 AlFn(n-3)-,可以推知n=6。
(5)晶胞中与体心亚铁离子位于距离相等并且最近的亚铁离子位于棱上共有12个;假设1mol Fe0.98Y中包含了Fe2+ x mol,Fe3+ y mol,x+y=0.98,阴阳离子电荷守恒2x+3y=2,两个方程联立解得x=0.94,y=0.04,n(Fe2+) : n(Fe3+)=0.94:0.04=47:2。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库。下图是从海水中提取食盐和溴的主要流程。

(1)粗盐除含 NaCl 外,还含有少量 MgCl2、 CaCl2、 Na2SO4以及泥沙等杂质。以下是粗盐提纯的
操作流程。

提供的试剂:
Na2CO3溶液、 K2CO3溶液、 NaOH 溶液、 BaCl2溶液、 Ba(NO3)2溶液、饱和 NaCl 溶液。
①除去溶液 I 中的 MgCl2、 CaCl2、 Na2SO4,从提供的试剂中选出 a 所代表的试剂,按滴加顺序依次为: 过量的NaOH 溶液、_______、_______;
②如何证明操作①中 NaOH 溶液已经过量?_______。
③蒸发过程所用的主要仪器有:铁架台、酒精灯、_______;
(2)某同学在实验室中用四氯化碳萃取较高浓度的溴水中的溴,经振荡并在铁架台上静置分层后,
①分离出四氯化碳层的操作是:_______。
②分离溴的四氯化碳溶液的操作方法是:_______。
(3)工业上将较高浓度的溴水经进一步处理得到工业溴。某研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料, Br2的沸点为 59℃,微溶于水,有毒性和强腐蚀性。水的沸点为 100℃。他们参观生产过程后,设计了如下装置简图:

①图中仪器 B 的名称:_______。
②用热水浴加热的优点是:_______。
③实验装置气密性良好,要达到提纯溴的目的,收集溴时温度计应控制的温度为:_______℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铝土矿为原料,提取氧化铝,冶炼铝的工艺流程如下图,下列说法错误的是( )
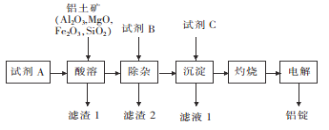
已知:滤渣2主要成分是Mg(OH)2、Fe(OH)3。
A. 试剂A可以是稀硫酸或盐酸B. 加入试剂B除去Mg2+、Fe3+
C. 滤渣1主要成分是SiO2D. 试剂C应是NH3或氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁单质及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料,其中发生的一个反应为3FeS2+8O2![]() 6SO2+Fe3O4,若有3 mol FeS2参加反应,则转移_______mol电子。
6SO2+Fe3O4,若有3 mol FeS2参加反应,则转移_______mol电子。
(2)氯化铁溶液常用作印刷电路铜板的腐蚀剂,反应的离子方程式为________________。从腐蚀废液中回收金属铜还需要的试剂是__________。
(3)与明矾相似,硫酸铁也可用于净水,其作用原理是____________________(用离子方程式表示);在使用时发现硫酸铁并不能使酸性废水中悬浮物沉降除去,其原因是_______________。
(4)铁红是一种红色颜料,其主要成分是Fe2O3。将一定量的铁红溶于160 mL 5 mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24 L氢气(标准状况),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理或实验操作正确的是( )
A.利用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体
B.只能利用焰色反应可鉴别KCl溶液和Na2SO4溶液
C.用润湿的pH试纸测量某溶液的pH
D.实验室用NaOH溶液除去CO2中的少量HCl气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示五层膜材料常用于汽车玻璃中的电致变色系统,其工作原理是在外接电源下,通过在膜材料内部发生氧化还原反应,实现对器件的光透过率进行多级可逆性调节。(已知:WO3和Li4Fe4[Fe(CN)6]3均为无色透明,LiWO3和Fe4[Fe(CN)6]3均为蓝色)下列有关说法正确的是( )

A. 当B外接电源负极时,膜的透射率降低,可以有效阻挡阳光
B. 当A接电源的正极时,此时Li+脱离离子存储层
C. 当B外接电源正极时,离子储存层发生反应为:Fe4[Fe(CN)6]3+4Li++4eˉ=Li4Fe4[Fe(CN)6]3
D. 该电致变色系统在较长时间的使用过程中,离子导体层中Li+的量可保持基本不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.SO2可用于漂白纸浆和草帽
B.Fe2O3可用作红色油漆和涂料
C.活性炭可用于去除冰箱中的异味
D.根据是否产生丁达尔效应,将分散系分为溶液,浊液和胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联合国将2019年定为“国际化学元素周期表年”,2018年中国化学会制作了新版周期表,包含118种元素。回答下列问题:

(1)碳元素在周期表中的位置是______________。
(2)将硅的元素符号填写在上述周期表相应的空格中。________
(3)在上述周期表中,用实线画出周期表的上方边界。_______
(4)第118号元素为Og(中文名“![]() ”,ào),下列说法不正确的是____。
”,ào),下列说法不正确的是____。
a.Og是第七周期0族元素
b.Og原子的核外有118个电子
c.Og在同周期元素中非金属性最强
d.中子数为179的Og核素符号是![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com