
【题目】下列有关实验原理或实验操作正确的是( )
A.利用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体
B.只能利用焰色反应可鉴别KCl溶液和Na2SO4溶液
C.用润湿的pH试纸测量某溶液的pH
D.实验室用NaOH溶液除去CO2中的少量HCl气体
科目:高中化学 来源: 题型:
【题目】一种瑞香素的衍生物的结构简式如图,下列有关该有机物性质的说法正确的是

A. 不能与FeCl3溶液发生显色反应
B. 1 mol该有机物最多可与3 mol H2加成
C. 1 mol该有机物最多可与含5 mol NaOH溶液反应
D. 1 mol该有机物与足量NaHCO3溶液反应可放出3 mol CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为 40%,且其核内质子数等于中子数。化合物R是由A、D两元素形成的离子化合物,其中A+阳离子与Dn-阴离子数之比为2∶1。请回答下列问题:
(1)B-的电子排布式为______________,在CB3分子中C元素原子的原子轨道发生的是______杂化。
(2)C的氢化物的空间构型为________________,其氢化物在同族元素所形成的氢化物中沸点最高的原因是__________________________________________________________。
(3)B元素的电负性____D元素的电负性(填“>”、“<”或“=”),用一个化学方程式说明B、D两元素形成的单质的氧化性强弱:________________________________。
(4)如图所示是R形成的晶体的晶胞,设晶胞的棱长为a cm。 试计算R晶体的密度为_________________。(阿伏加德罗常数用NA表示)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝及其化合物广泛应用于金属冶炼和有机合成等领域。
(1)铝热反应可以冶炼金属铬,基态铬原子的核外电子排布式为:_______________________。
(2)AlCl3可用作下列反应的催化剂

①乙酸酐分子中发生sp3杂化的原子共有______个
②CH3COOH和H2O可以以任意比例互溶,其原因是它们均是极性分子和_________________。
③单个AlCl3分子的空间构型为_______。
(3)在氧化铝的作用下,N4H4(SO4)2可同碱反应生成一种类似白磷的N4分子,1molN4分子中含有的共价键的物质的量为_____mol
(4)某遮光剂的晶胞如图甲(黑球为Na+,白球为AlFn(n-3)-阴离子),由图可推算知,n=________。

(5)由Fe和Y形成的某化合物的晶胞如图乙所示,该晶胞中与亚铁离子距离相等并且最近的亚铁离子有_____个。 另有一种有缺陷的Fe和Y形成的化合物的晶体由Fe2+,Fe3+,Y2-及空隙组成,可表示为Fe0.98Y,则该晶体中,n(Fe2+) : n(Fe3+) =______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 毒胶囊和老酸奶事件说明化学试剂对食品的危害,我们应该拒绝一切化学试剂的使用
B. 兴建更多的钢铁、水泥企业,提高钢铁、水泥的产量
C. 日本核泄漏造成的核辐射事故暴露出核能应用潜在的巨大危险,应立即停建核电站
D. 开发新能源,减小含碳化合物的使用,降低碳的排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在3个体积均为1 L的恒容密闭容器中发生反应:SO2(g)+2NO(g)![]() 2NO2(g)+S(s)。改变容器I的反应温度,平衡时c( NO2)与温度的关系如下图所示。下列说法正确的是
2NO2(g)+S(s)。改变容器I的反应温度,平衡时c( NO2)与温度的关系如下图所示。下列说法正确的是
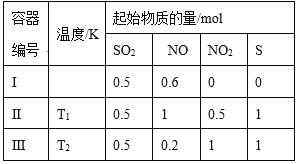
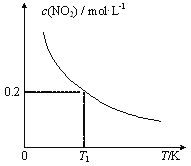
A. 若T2<T1,达到平衡时,容器Ⅲ中NO的体积分数小于40%
B. 该反应的ΔH>0
C. T1时,该反应的平衡常数为![]()
D. 容器Ⅰ与容器Ⅱ均在T1时达到平衡,总压强之比小于1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质或应用的说法正确的是( )
A.晶体硅是半导体,故在通信工程中用于制光导纤维
B.氧化镁的熔点高,可作优质的耐高温材料
C.液氨汽化放出大量的热,可用作制冷剂
D.明矾具有强氧化性,常用于自来水的杀菌消毒
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com