
分析 求出氢氧化钠的物质的量,然后根据物质的量浓度c=$\frac{n}{V}$来计算;由于氢氧化钠是一元强碱,故所得溶液中c(OH-)=c(NaOH),然后根据c(H+)=$\frac{Kw}{c(O{H}^{-})}$来计算,而溶液的pH=-lgc(H+)计算.
解答 解:0.4g氢氧化钠的物质的量n=$\frac{0.4g}{40g/mol}$=0.01mol,由于溶液体积为1L,故溶液的物质的量浓度c=$\frac{n}{V}$=$\frac{0.01mol}{1L}$=0.01mol/L;由于氢氧化钠是一元强碱,故所得溶液中c(OH-)=c(NaOH)=0.01mol/L,故c(H+)=$\frac{Kw}{c(O{H}^{-})}$=$\frac{1{0}^{-14}}{0.01}$=10-12mol/L,溶液的pH=-lgc(H+)=-lg10-12=12.故答案为:0.01mol/L;10-12mol/L;12.
点评 本题考查了所配置溶液的物质的量浓度和离子浓度以及溶液pH的有关计算,难度不大,注意掌握公式的运用.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
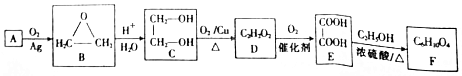
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和乙醚互为同分异构体 | |
| B. | 乙醇和乙二醇互为同系物 | |
| C. | 含羟基的化合物一定属于醇类 | |
| D. | 等质量的乙醇、乙二醇与足量钠反应时,乙二醇产生的氢气的量较乙醇的多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应的△S<0 | B. | 该反应的△H<0 | ||
| C. | 该反应是不可逆反应 | D. | 该反应产物不会造成大气污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ag+、Na+、CO32- | B. | H+、Fe2+、Cl- | C. | Cu2+、H+、SO42- | D. | Ba2+、H+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L | B. | 0.05mol/L | C. | 0.2mol/L | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
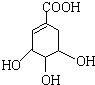 莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一.莽草酸是A的一种异构体.A的结构简式如下:
莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一.莽草酸是A的一种异构体.A的结构简式如下: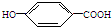 ),其反应类型是消去反应,化学方程式是
),其反应类型是消去反应,化学方程式是 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$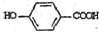 +2H2O.
+2H2O. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com