
分析 (1)醋酸根离子水解溶液呈碱性,溶液呈红色;
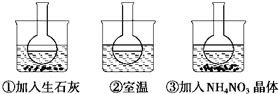
(2)如图所示三个烧瓶中分别装入含酚酞的0.01mol•L-1CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰与水反应生成氢氧化钙,放热,溶液红色加深,向烧杯③中加入NH4NO3晶体溶解后,铵根离子水解显酸性,和氢氧根离子反应促进醋酸根离子水解,溶液碱性减弱,颜色变浅;烧杯②中不加任何物质,醋酸根离子水解溶液呈碱性,溶液呈红色;
(3)依据醋酸根离子水解平衡的影响因素判断平衡移动方向.
解答 解:(1)醋酸根离子水解结合水电离出的氢离子,促进水电平衡正向进行,氢氧根离子浓度增大溶液呈碱性,遇到酚酞溶液呈红色,CH3COO-+H2O?CH3COOH+OH- 使溶液显碱性,
故答案为:醋酸根离子水解结合水电离出的氢离子,CH3COO-+H2O?CH3COOH+OH-,促进水的电离平衡正向进行,溶液中氢氧根离子浓度增大,使溶液显碱性;
(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,向烧杯①中加入生石灰与水反应生成氢氧化钙,放热,溶液红色加深,向烧杯③中加入NH4NO3晶体溶解后,铵根离子水解显酸性,和氢氧根离子反应促进醋酸根离子水解,溶液碱性减弱,颜色变浅;
A、水解反应是吸热反应,故A错误;
B、水解反应是吸热反应,故B正确;
C、NH4NO3溶于水时吸热,故C错误;
D、NH4NO3溶于水时吸收热量,故D正确;
故答案为:BD;
(3)向0.01mol•L-1CH3COONa溶液中存在水解平衡,CH3COO-+H2O?CH3COOH+OH- 使溶液显碱性,加入NaOH固体溶解后溶液中氢氧根离子浓度增大,抑制水解平衡,平衡左移,
故答案为:左.
点评 本题考查了盐类水解的应用,水解平衡的影响因素因素分析判断,物质溶解过程的特征变化,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 国庆期间燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 | |
| B. | 二氧化硅可以用来制光导纤维 | |
| C. | 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶 | |
| D. | 青铜是我国使用最早的合金材料,目前世界上使用量最大的合金材料是钢铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫粉在过量的纯氧中燃烧可以生成SO3 | |
| B. | 可用苯萃取碘水中的碘,再用长颈漏斗进行分液,即可实现分离 | |
| C. | 氢氧化铁胶体带正电,土壤胶体带负电 | |
| D. | 铁粉与过量硫粉反应生成硫化亚铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业” | |
| B. | 用二氧化锰和浓盐酸制取氯气,每生成1 mol氯气被氧化的氯化氢为4 mol | |
| C. | 过量的铁与氯气反应时生成氯化亚铁 | |
| D. | 工业上以氯气和石灰石直接反应制造漂白粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冰醋酸中醋酸分子之间 | |
| B. | 可燃冰(CH4•8H2O)中甲烷分子与水分子之间 | |
| C. | 液态氟化氢中氟化氢分子之间 | |
| D. | 一水合氨分子中的氨分子与水分子之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,20mlNH3与60mlO2所含分子个数比为1:3 | |
| B. | 将80克NaOH溶于1L水中,所得溶液的物质的量浓度为2mol/L | |
| C. | 标准状况下,1molSO3的体积约是22.4L | |
| D. | 在常温、常压下,11.2LN2含有的分子数为0.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com