
【题目】在一块表面无锈的铁片上滴食盐水,放置一段时间后看到铁片上有铁锈出现.铁片腐蚀过程中发生的总化学方程式:2Fe+2H2O+O2═2Fe(OH)2 , Fe(OH)2进一步被氧气氧化为Fe(OH)3 , 再在一定条件下脱水生成铁锈,其原理如图.下列说法正确的是( ) 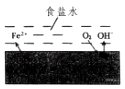
A.铁片发生还原反应而被腐蚀
B.此过程中电子从C移向Fe
C.铁片腐蚀中负极发生的电极反应:2H2O+O2+4e﹣═4OH﹣
D.铁片里的铁和碳与食盐水形成无数微小原电池,发生了电化学腐蚀
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O).下列说法正确的是( ) 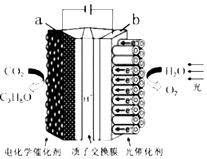
A.a电极的反应为:3CO2+18H++18e﹣=C3H8O+5H2O
B.该装置工作时,H+从b极区向a极区迁移
C.每生成1molO2 , 有44gCO2被还原
D.该装置将化学能转化为光能和电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y ![]() 2Z,其平衡常数为1600
2Z,其平衡常数为1600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.化学实验室中的蔗糖纯度很高,可以用来食用
B.实验室中制取完有毒气体,开窗通风即可
C.实验室中用过的废洗液,可以用来冲洗厕所
D.不能用手接触药品,不要把鼻孔凑到容器口去闻药品的气味,不得尝任何药品的味道
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列做法不存在安全隐患的是
A.氢气还原氧化铜实验中,先加热氧化铜后通氢气
B.实验室做钠的实验时,余下的钠屑投入到废液缸中
C.制乙烯时,用量程为300 ℃的温度计代替量程为200 ℃的温度计,测反应液的温度
D.蒸馏石油时,加热一段时间后发现未加碎瓷片,立刻拔开橡皮塞并投入碎瓷片
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式中正确的是( )
A.NaHSO4溶于水:NaHSO4Na++H++SO42﹣
B.次氯酸电离:HClO═ClO﹣+H+
C.HF溶于水:HF+H2OH3O++F﹣
D.NH4Cl溶于水:NH4++H2ONH3H2O+H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些补铁剂的成分中含有硫酸亚铁,长期放置会因氧化而变质。检验硫酸亚铁是否变质的试剂是
A. 稀盐酸 B. 石蕊溶液 C. KSCN溶液 D. 氯水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学反应A(g)+3B(g)2C(g)+D(g)中,各物质的平均反应速率间的关系式正确的是( )
A.vA=vB
B.vA=2vC
C.3vB=vC
D.vB=3vD
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管后立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答:
(1)以上操作步骤中有一步有错误,请指出编号 ,该错误操作会导
致测定结果 (填“偏大”、“偏小”或“无影响”)
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入 中。(从右图中选填“甲”或“乙”)

(3)下列操作会引起实验结果偏大的是: (填编号)
A.在锥形瓶装液前,留有少量蒸馏水 |
B.滴定前,碱式滴定管尖嘴有气泡,滴定后无气泡 |
C.锥形瓶先用蒸馏水洗涤后,再用待测液润洗 |
D.用酸式滴定管量取待测液时将一滴待测液滴在锥形瓶外 |
(4)判断到达滴定终点的现象是:锥形瓶中溶液从 色变为 色,且半分钟之内不再改变。
(5)以下是实验数据记录表

通过计算可得,该盐酸浓度为: mol·L-1(计算结果保留2位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com