
����Ŀ��ijѧ����0.2000mol��L��1�ı�NaOH��Һ�ζ�δ֪Ũ�ȵ����ᣬ������ɷ�Ϊ���¼�����
��������ˮϴ�Ӽ�ʽ�ζ��ܺ�����ע��NaOH��Һ����0���̶������ϣ�
���̶��õζ��ܲ�ʹ�ζ��ܼ������Һ�壻
������Һ������0������0���̶������£������¶�����
����ȡ20.00mL����Һע��ྻ����ƿ�У�������3�η�̪��Һ��
���ñ�Һ�ζ����յ㣬���µζ���Һ�������
��ش�
��1�����ϲ�����������һ���д���,��ָ����� ���ô�������ᵼ
�²ⶨ��� (����ƫ��������ƫС��������Ӱ����)
��2���ñ�NaOH��Һ�ζ�ʱ��Ӧ����NaOH��Һע�� �С�������ͼ��ѡ������������������

��3�����в���������ʵ����ƫ����ǣ� �����ţ�
A������ƿװҺǰ��������������ˮ |
B���ζ�ǰ����ʽ�ζ��ܼ��������ݣ��ζ��������� |
C����ƿ��������ˮϴ�Ӻ����ô���Һ��ϴ |
D������ʽ�ζ�����ȡ����Һʱ��һ�δ���Һ������ƿ�� |
��4���жϵ���ζ��յ�������ǣ���ƿ����Һ�� ɫ��Ϊ ɫ���Ұ����֮�ڲ��ٸı䡣
��5��������ʵ�����ݼ�¼��

ͨ������ɵã�������Ũ��Ϊ�� mol��L��1������������2λС������
���𰸡���1������ƫ��2���ң���3��BC����4���ޣ�dz�죻��5��0.16
�������������������1����ʽ�ζ�����װҺǰӦ�ô�װҺ������ϴ�������������������б��������������ˮϴ�Ӽ�ʽ�ζ��ܣ�������ע��NaOH��Һ����0���̶������ϣ���ʽ�ζ���δ�ñ�NaOH��Һ��ϴ��ֱ��ע���NaOH��Һ����Һ��Ũ��ƫС�����V������ƫ��������ҺŨ��ƫ��
��2��NaOH��ҺӦʢװ�ڼ�ʽ�ζ����У�ѡ�ҡ�
��3��A������ƿװҺǰ��������������ˮ��V���������䣬�Բⶨ�����Ӱ�죬A�����B���ζ�ǰ����ʽ�ζ��ܼ��������ݣ��ζ��������ݣ����±�Һ���������������ҺŨ��ƫ��B����ȷ��C����ƿ��������ˮϴ�Ӻ����ô���Һ��ϴ���������ı�Һ���������������ҺŨ��ƫ��C����ȷ��D������ʽ�ζ�����ȡ����Һʱ��һ�δ���Һ������ƿ�⣬���´���Һ��С�����ı�Һ��������٣�������ҺŨ��ƫС��D�����ѡBC��
��4���ζ�ʱ������Һ��ɫ�仯�Ұ�����ڲ���ɫ����˵���ﵽ�ζ��յ㣬���Ե��������һ��NaOH��Һ����Һ����ɫ��Ϊdz��ɫ���Ұ�����ڲ��ٸı䡣
��5��2��NaOH��Һ�����ƽ��ֵΪ��16.30+16.22����2=16.26mL��c�����⣩=(0.2000mol��L��1��16.26mL )��20.00mL=0.16molL-1��


 �ʰ�Ӣ��ͬ����ϰ��ϵ�д�
�ʰ�Ӣ��ͬ����ϰ��ϵ�д� ѧϰʵ����ϵ�д�
ѧϰʵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������������Ƭ�ϵ�ʳ��ˮ������һ��ʱ�����Ƭ����������֣���Ƭ��ʴ�����з������ܻ�ѧ����ʽ��2Fe+2H2O+O2�T2Fe��OH��2 �� Fe��OH��2��һ������������ΪFe��OH��3 �� ����һ����������ˮ�������⣬��ԭ����ͼ������˵����ȷ���ǣ� �� 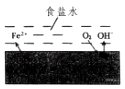
A.��Ƭ������ԭ��Ӧ������ʴ
B.�˹����е��Ӵ�C����Fe
C.��Ƭ��ʴ�и��������ĵ缫��Ӧ��2H2O+O2+4e���T4OH��
D.��Ƭ�������̼��ʳ��ˮ�γ�����Сԭ��أ������˵绯ѧ��ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ����֤ľ̿�ɱ�ŨH2SO4������CO2 �� ѡ����ͼ��ʾ�������ں����ʣ���װ��ʵ��װ�ã� 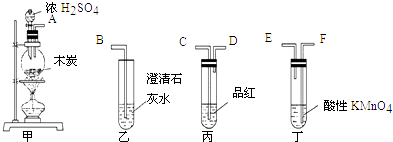
��1���簴������������������������װ�õ���ȷ˳���ǣ�����ӿ���ĸ������ �� �� �� ����
��2�������ҡ���Ӧ��������ʵ������ű����Ѽ����CO2������ �� ������
��3����������KMnO4��Һ����������
��4��д�����з�Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵĵ���ƽ�⡢�����ˮ��ƽ�����������ܽ�ƽ������ڻ�ѧƽ�⡣
��.��֪H2A��ˮ�д�������ƽ�⣺H2A=H++HA-��HA-![]() H++A2-
H++A2-
��1��ij�¶��£�����0.1mol��L-1��NaHA��Һ����εμ�0.1 mol��L-1 KOH��Һ����Һ������(���Ի�Ϻ���Һ������仯)����ʱ�û����Һ�е����й�ϵһ����ȷ����__________��
A.c(H+)��c(OH-)=l.0��10-14
B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+)
D.c(Na+)+c(K+)=0.05mol��L-1
��2����֪������H2A�ĸ���(CaA)�ı�����Һ�д�������ƽ�⣺CaA(s)![]() Ca2+(aq)+A2+(aq) ��H>0����Ҫʹ����Һ��Ca2+Ũ�ȱ�С���ɲ�ȡ�Ĵ�ʩ��____________��
Ca2+(aq)+A2+(aq) ��H>0����Ҫʹ����Һ��Ca2+Ũ�ȱ�С���ɲ�ȡ�Ĵ�ʩ��____________��
A.�����¶� B.�����¶�
C.����NH4Cl���� D.����Na2A����
��.����Cr2O72-�ķ�ˮ���Խϴ�ij������ˮ�к�5.0��10-3mol��L-1��Cr2O72-��Ϊ��ʹ��ˮ���ŷŴ�꣬�������´�����
![]()
��1���÷�ˮ�м����̷���H+��������Ӧ�����ӷ���ʽΪ________________________��
��2����������ķ�ˮ�в�����c(Fe3+)=2.0��10-13mol��L-1���������Cr3+��Ũ��Ϊ___________��(��֪��Ksp[Fe(OH)3)]=4.0��10-38�� Ksp[Cr(OH)3]=6.0��10-31)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڸ����������£�����ѡ����ʾ�����ʼ�ת������ʵ�ֵ��ǣ� ��
A.SiO2 ![]() SiCl4
SiCl4 ![]() Si
Si
B.FeS2 ![]() SO2
SO2 ![]() H2SO4
H2SO4
C.N2 ![]() NH3
NH3 ![]() NH4Cl��aq��
NH4Cl��aq��
D.MgCO3 ![]() MgCl2��aq��
MgCl2��aq�� ![]() Mg
Mg
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ�������������ij�����غϳɹ����е��м�������˵����ȷ���ǣ� �� 
A.�ҡ������ܷ���������Ӧ
B.��FeCl3��Һ����ס��������л�������
C.����������̼ԭ�ӿ��ܹ�ƽ��
D.�ס��ҡ��������л������������NaOH��Һ������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ˮ�����������Ȼ�̼�;ƾ��ҵ�����������Ҫ����ˮ�еĵ�������������˵����������
A�������������ɲ��ü��ȵķ����������Һ����������
B�������������Ȼ�̼�;ƾ������Կ�ѡ�������Լ��е�����һ�ֽ�����ȡ
C�����Ȼ�̼��ˮ�أ��ƾ���ˮ�ᣬ���������Ȼ�̼������ȡ���þƾ���
D�����Ȼ�̼������ˮ���ƾ�����ˮ�����������Ȼ�̼��ȡ�������þƾ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʮ��������ѧ�����߶�̼�����������˹㷺������о���ȡ����һЩ��Ҫ�ɹ���������CO2��CH4�������ƺϳ�������Ҫ�ɷ�ΪCO��H2������֪���������в��ַ�Ӧ���Ȼ�ѧ����ʽΪ��
I��CH4��g���TC��s��+2H2��g����H=+75.0kJmol��1
II��CO2��g��+H2��g���TCO��g��+H2O��g����H=+41.0kJmol��1
III��CO��g��+H2��g���TC��s��+H2O��g����H=��131.0kJmol��1
��1����ӦCO2��g��+CH4��g���T2CO��g��+2H2��g���ġ�H=kJmol��1 ��
��2���̶�n��CO2��=n��CH4�����ı䷴Ӧ�¶ȣ�CO2��CH4��ƽ��ת���ʼ�ͼ�ף� 
��ͬ�¶���CO2��ƽ��ת����������ڡ���С�ڡ���CH4��ƽ��ת���ʣ���ԭ����
�ڸ����½��и÷�Ӧʱ������ӦI���ɡ���̼����̼���ʣ�����ɴ����ж��������·�ӦI���Է����е�ԭ���� ��
��3��һ��������Pd��Mg/SiO2������ʹCO2�����黯���Ӷ����Ϊ�����䷴Ӧ������ͼ����ʾ���÷�Ӧ�Ļ�ѧ����ʽΪ
��4��CO�����ڹ�ҵұ����������ͼ���ڲ�ͬ�¶���CO��ԭ���ֽ����������ƽ���������lg[c��CO��/c��CO2��]���¶ȣ�t���Ĺ�ϵ����ͼ������˵����ȷ����
A.��ҵ�Ͽ���ͨ�����߷�Ӧװ�����ӳ���ʯ��
CO�Ӵ���ʱ�䣬����β����CO�ĺ���
B.CO���������ڹ�ҵұ����������Cr��
C.��ҵұ������ͭ��Cu��ʱ�ϵ͵��¶�������
���CO��������
D.CO��ԭPbO2�ķ�Ӧ��H��0
��5�������˺�������Ӧ�õ绯ѧԭ������PtΪ������Pb��CO2�����壩Ϊ������KHCO3��ҺΪ�������Һ����ԭ������������CO2ͬʱ����O2���µ���ԴCO���ܷ�Ӧ�Ļ�ѧ����ʽΪ��2CO2 ![]() 2CO+O2 �� ���������ĵ缫��ӦʽΪ ��
2CO+O2 �� ���������ĵ缫��ӦʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ18��������Ϊ10; X��Neԭ�ӵĺ�����������1; Y�ĵ�����һ�ֳ����İ뵼������� Z�ķǽ�������ͬ����Ԫ������ǿ������˵����ȷ����

A. ��Ӧ�����Ӱ뾶�� X>W
B. ��Ӧ��̬�⻯����ȶ���Y
C. ������XZW�Ⱥ����Ӽ����ֺ����ۼ�
D. Y�����������ҵ��⻯�X������������Ӧ��ˮ�������Һ���ܷ�Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com