
【题目】甲、乙、丙三种物质是某抗生素合成过程中的中间产物,下列说法正确的是( ) 
A.乙、丙都能发生银镜反应
B.用FeCl3溶液鉴别甲、丙两种有机化合物
C.甲分子中所有碳原子可能共平面
D.甲、乙、丙三种有机化合物均可与NaOH溶液发生反应
【答案】BC
【解析】解:A.醛基能发生银镜反应,乙含有醛基,能发生银镜反应,丙不含醛基,不能发生银镜反应,故A错误;
B.氯化铁能和酚发生显色反应,甲不含酚羟基而丙含有酚羟基,则丙能发生显色反应,而甲不能发生显色反应,所以可以用氯化铁溶液鉴别甲、丙,故B正确;
C.苯环为平面形结构,与苯环直接相连的原子共平面,且甲中C﹣O键可旋转,C有可能与苯环在同一个平面上,故C正确;
D.酚羟基、羧基、卤原子或酯基都能和NaOH溶液反应,甲中不含酚羟基、羧基、卤原子或酯基,所以不能和NaOH溶液反应,故D错误.
故选BC.
【考点精析】本题主要考查了有机物的结构和性质的相关知识点,需要掌握有机物的性质特点:难溶于水,易溶于汽油、酒精、苯等有机溶剂;多为非电解质,不易导电;多数熔沸点较低;多数易燃烧,易分解才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】下列电离方程式中正确的是( )
A.NaHSO4溶于水:NaHSO4Na++H++SO42﹣
B.次氯酸电离:HClO═ClO﹣+H+
C.HF溶于水:HF+H2OH3O++F﹣
D.NH4Cl溶于水:NH4++H2ONH3H2O+H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】进行过滤操作时应选用的一组仪器及用品是
A.玻璃棒、滤纸、烧瓶、漏斗、铁架台
B.滤纸、烧杯、试管夹、漏斗、玻璃棒
C.漏斗、玻璃棒、烧杯、铁架台、滤纸
D.烧杯、酒精灯、试管、铁架台、漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管后立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答:
(1)以上操作步骤中有一步有错误,请指出编号 ,该错误操作会导
致测定结果 (填“偏大”、“偏小”或“无影响”)
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入 中。(从右图中选填“甲”或“乙”)

(3)下列操作会引起实验结果偏大的是: (填编号)
A.在锥形瓶装液前,留有少量蒸馏水 |
B.滴定前,碱式滴定管尖嘴有气泡,滴定后无气泡 |
C.锥形瓶先用蒸馏水洗涤后,再用待测液润洗 |
D.用酸式滴定管量取待测液时将一滴待测液滴在锥形瓶外 |
(4)判断到达滴定终点的现象是:锥形瓶中溶液从 色变为 色,且半分钟之内不再改变。
(5)以下是实验数据记录表

通过计算可得,该盐酸浓度为: mol·L-1(计算结果保留2位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用浓度为0.1000molL﹣1的NaOH溶液分别逐滴加入到20.00mL 0.1000molL﹣1的HX,HY溶液中,pH随NaOH溶液体积的变化如图.下列说法正确( ) 
A.V(NaOH)=10.00 mL时,c(X﹣)>c(Na+)>c(H+)>c(OH﹣)
B.V(NaOH)=20.00 mL时,两份溶液中,c(X﹣)>c(Y﹣)
C.V(NaOH)=20.00 mL时,c(Na+)>c(X﹣)>c(OH﹣)>c(H+)
D.pH=7时,两份溶液中,c(X﹣)=c(Y﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F是一种治疗关节炎止痛药,合成F的一种传统法路线如图: 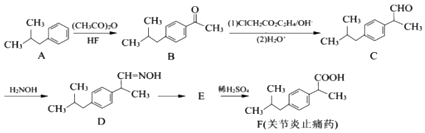
已知:① ![]() ;②
;② ![]() ; ③
; ③ ![]() .
.
(1)B中含氧官能团的名称为 .
(2)已知D经过反应可生成E,E的分子式C13H17N,写出E的结构简式 .
(3)A→B的反应类型为、A→B的反应方程式为 .
(4)写出同时满足下列条件的F的一种同分异构体的结构简式:(写一种).
①能发生银镜反应;②能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应;③分子中只有4种不同化学环境的氢.
(5)合成F( ![]() )的一种改良法是以2﹣甲基﹣1﹣丙醇(
)的一种改良法是以2﹣甲基﹣1﹣丙醇( ![]() )、苯、
)、苯、
乙酸酐[(CH3CO)2O]为原料来合成,写出有关F的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
H2C=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH .
CH3CH2OH .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,向某V L的密闭容器中充入3molH2(g)和3molI2(g),发生反应:
H2(g)+I2(g)2HI(g)△H=﹣26.5kJmol﹣1 ,
测得各物质的物质的量浓度与时间变化的关系如图所示.请回答下列问题:
(1)V=L.
(2)该反应达到最大限度的时间是S,该时间内平均反应速率v(HI)=mol/(Ls).
(3)该反应达到平衡状态时,(填“吸收”或“放出”)的热量为kJ.
(4)判断该反应达到平衡的依据是(填序号).①H2消耗的速率和I2消耗的速率相等 ②H2、I2、HI的浓度比为1:1:2
③H2、I2、HI的浓度都不再发生变化④该条件下正、逆反应速率都为零
⑤混合气体的平均分子量不再发生变化 ⑥气体的颜色不再发生变化.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能大量共存于同一溶液中的离子组是
A. Ca2+、NO3—、Cl—
B. Ba2+、K+、SO42—
C. Na+、Mg2+、OH—
D. H+、Cl—、OH—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com